2020.05.02.14
Files > Volume 5 > Vol 5 No 2 2020
REVISION/REVIEW
LOX-1 en las afecciones cardiovasculares, perspectivas terapéuticas futuras.
LOX-1 in cardiovascular diseases, future therapeutic perspectives.
Thelvia I. Ramos Gómez 1*, Jorge Roberto Toledo Alonso 2
Available from: http://dx.doi.org/10.21931/RB/2020.05.02.14
RESUMEN
El receptor de la lipoproteína de baja densidad oxidado tipo lectina 1 (LOX-1), también conocido como OLR-1, es un receptor scavenger (SR) clase E, que media la absorción del colesterol LDL en su forma oxidada, por las células vasculares. LOX-1 está involucrado en la disfunción endotelial, la adhesión de monocitos, la proliferación, migración y apoptosis de las células del músculo liso, la formación de células espumosas, la activación de plaquetas, así como la inestabilidad a nivel del endotelio vascular; todos eventos críticos en la patogénesis de la aterosclerosis. LOX-1 contribuyen a la inestabilidad de la placa ateroesclerótica y a las últimas secuelas clínicas de ruptura endotelial e isquemia tisular cardíaca potencialmente mortal. No existe en la actualidad ningún fármaco aprobado o en desarrollo clínico a partir de LOX-1, debido a sus complejos mecanismos biológicos no dilucidados completamente. Se han utilizado diversas terapias con el objetivo de inhibir la acción de LOX-1; medicamentos como: antioxidantes, estatinas, agentes antinflamatorios naturales, que actúen sobre su expresión, pero todos con eficacia moderada. También se ha evaluado la administración de anticuerpos anti-LOX-1 inhibe la aterosclerosis al disminuir eventos celulares. El diseño de fármacos enfocados en el conocimiento de las vías de señalización de LOX-1 y la aplicación de herramientas biotecnológicas permite el desarrollo de nuevas dianas terapéuticas basadas en la potencialidad que tienen los anticuerpos monoclonales. Con estos antecedentes el, receptor LOX-1, representa un objetivo terapéutico atractivo para el tratamiento de enfermedades ateroscleróticas humanas. La evidencia reciente indica que la acción sobre este SR es una posible estrategia para el tratamiento de la enfermedad vascular, explorando en esta revisión su papel y posibles futuras aplicaciones en el diagnóstico y la terapéutica.
Palabras claves: Ateroesclerosis; LOX-1 receptor de la lipoproteína de baja densidad oxidado tipo lectina 1; Dislipidemia; Disfunción endotelial; lipoproteína de baja densidad oxidado (ox-LDL); forma soluble LOX-1 (sLOX-1).
SUMMARY
The low-density oxidized lipoprotein lectin-1 (LOX-1) receptor, also known as OLR-1, is a scavenger receptor (SR) class E, which mediates the absorption of LDL cholesterol in its oxidized form by vascular cells. LOX-1 is involved in endothelial dysfunction, monocyte adhesion, smooth muscle cell proliferation, migration and apoptosis, foam cell formation, platelet activation, and vascular endothelial instability, all critical events in the pathogenesis of atherosclerosis. LOX-1 contributes to atherosclerotic plaque instability and the ultimate clinical sequelae of endothelial rupture and potentially fatal cardiac tissue ischemia. There is currently no drug approved or in clinical development from LOX-1, due to its complex biological mechanisms not fully elucidated. Various therapies have been used to inhibit the action of LOX-1; drugs such as antioxidants, statins, natural anti-inflammatory agents, which act on its expression, but all with moderate efficacy. The administration of anti-LOX-1 antibodies has also been evaluated to inhibit atherosclerosis by decreasing cellular events. The design of drugs focused on the knowledge of LOX-1 signaling pathways and the application of biotechnological tools allow the development of new therapeutic targets based on the potential of monoclonal antibodies. With this background, the LOX-1 receptor represents an attractive therapeutic target for the treatment of human atherosclerotic diseases. Recent evidence indicates that action on this SR is a possible strategy for the treatment of vascular disease, exploring in this review its role and potential future applications in diagnosis and therapy.
Keywords: Atherosclerosis; LOX-1 lectin-like OxLDL receptor 1; Dyslipidemia; Endothelial dysfunction; oxidized low-density lipoprotein; Soluble LOX-1.
INTRODUCCIÓN
Antecedentes
Las enfermedades cardiovasculares (ECVs) representan alrededor del 30% de defunciones a nivel global, siendo la principal causa de muerte en la población en general 1, consecuencia de tres afecciones subyacentes: el ataque cardíaco, el accidente cerebrovascular y enfermedad vascular periférica 2.
La aterosclerosis es la base fisiológica de las enfermedades cardiovasculares más peligrosas 3. Se desarrolla en la pared vascular de las arterias y arteriolas, y se describe por una acumulación local de colesterol, inflamación no resuelta, muerte celular y fibrosis 4. Es un proceso dinámico gradual con modificaciones estructurales multifocales, que da lugar al desarrollo de placas ateroscleróticas 5. Estas placas se asocian a disfunción y activación endotelial 6, 7, 8. Todo esto ocasiona una restricción del flujo, riesgo de rotura, ataque cardíaco o una isquemia a nivel vascular 9.
El factor de riesgo más importante para la aterosclerosis son los niveles elevados de colesterol LDL y su apolipoproteína B (apoB) 100, principal proteína estructural de colesterol-LDL 10 y específicamente su forma oxidada (ox-LDL) 11. Esta variante oxidada del colesterol LDL es mucho más importante en la aterogénesis que el colesterol LDL nativo no modificado 12.
La forma ox-LDL aumenta con la disfunción endotelial 13 y su presencia en la pared arterial conduce a la aterogénesis 14. Esta lipoproteína en su forma oxidada, ejerce diversos efectos sobre células endoteliales, plaquetas, macrófagos, fibroblastos y células del músculo liso (SMC), a través de la glucoproteína de transmembrana, el receptor de la lipoproteína de baja densidad oxidado tipo lectina 1 (LOX-1) 15.
La evidencia actual demuestra que ox-LDL inicia y sostiene la aterogénesis por activación LOX-1 16 y a nivel molecular la internalización de ox-LDL a la íntima de los vasos sanguíneos, se provoca por este receptor LOX-1 17, que establece una fuerte asociación sistema ligando-receptor 16. LOX-1 juega un rol crítico en la disfunción y daño endotelial, permitiendo el inicio y la progresión del proceso aterosclerótico y ha sido propuesto como una diana terapéutica para el desarrollo de una molécula recombinante dirigida al tratamiento de la aterosclerosis 18.
El receptor 1 de lipoproteína de baja densidad oxidada tipo lectina (LOX-1) se descubrió por primera vez como un receptor vascular para partículas de lipoproteína modificada 19. Desde entonces, los estudios in vitro/in vivo han demostrado su asociación con patologías como: aterosclerosis, artritis, hipertensión, hiperlipidemias y diabetes 20. Sin embargo, no existe en la actualidad ningún medicamento aprobado ni en ensayos clínicos a partir de LOX-1, debido a los complejos mecanismos fisiopatológicos e inmunológicos en los que se encuentra inmersa esta molécula.
Conocemos que la terapia basada en LOX-1 reduce la aterogénesis y anormalidades celulares asociadas y que su inhibición, mediante el uso de anticuerpos, podría influir sobre la lesión miocárdica 21. Toda la evidencia obtenida lo ha convertido en un objetivo potencialmente terapéutico para la aterosclerosis y las enfermedades cardiovasculares, debido a dos propiedades importantes: (1) Es un receptor de transmembrana, y los sitios de unión para ox-LDL y otros ligandos han sido bien caracterizados 22; (2) los mecanismos y las vías de señalización mediadas por LOX-1 son bien conocidos 23.
Existen avances en la fisiopatología de las enfermedades cardiovasculares en las últimas décadas 24–26. Varios medicamentos con impacto en los factores de riesgo coronario y la cardiopatía isquémica han sido estudiados inhibiendo la función de LOX-127.
Se requieren sistemas diagnósticos sólidos y nuevas terapias emergentes para las enfermedades cardiovasculares 28. Tenemos las bases para la formulación de nuevas moléculas, a través de la aplicación de las herramientas de la biotecnología molecular, que disminuyan los altos índices de las enfermedades cardiovasculares; y LOX-1 por sus particularidades y funciones biológicas, pudiera tener un impacto favorable sobre las terapias emergentes.
DESARROLLO
El receptor de la lipoproteína de baja densidad oxidado tipo lectina (LOX-1), es el principal responsable de la unión, internalización y degradación de la ox-LDL en células endoteliales 29. Tiene un papel protagónico en el desarrollo de la aterosclerosis y la enfermedad cardiovascular 30.
LOX-1 es un receptor scavenger (SR) de clase E, glicoproteína de membrana tipo II, que une carbohidratos dependiente Ca2+ 31. Perteneciente a la familia de receptores de lectina tipo C 32, se clonó por primera vez 15 e identificó como un receptor vascular endotelial de ox-LDL 33.
El gen de esta proteína (gen OLR1) se encuentra ubicado en el cromosoma humano 12 34 y su producto es un homodímero de 50 kDa 35 conformado por 273 aminoácidos que consta de cuatro dominios: un dominio de lectina extracelular tipo C-terminal principal responsable de su funcionalidad con 131 residuos (143-273), un dominio cuello de 82 aminoácidos (61-142), un solo dominio transmembrana o transcelular de 27 aminoácidos (34-61) y una cola citoplasmática N-terminal corta de 34 aminoácidos (1-34) (ver Figura 1) 36.

Figura 1. Receptor de la lipoproteína de baja densidad oxidado tipo lectina 1.
LOX-1 se comporta como un SR en la superficie celular y participa en la unión, endocitosis y degradación proteolítica de ox-LDL. Sin embargo, no comparte ninguna homología con otros SR 37. LOX-1 es sintetizado como un precursor (pre-LOX1) glicosilado con residuos de manosa, ligados el extremo N-terminal (40 kDa). Posteriormente, es procesado como una glicoproteína madura 38. Se identificó un sitio de glucosilación potencial en su forma recombinante en asparagina 139 (Asn-139) 39. Similar a otros receptores con un único dominio transmembrana, LOX-1 puede ser escindido por proteasas y secretado en forma soluble (sLOX-1) 40, a través de la escisión proteolítica de su dominio extracelular 28.
El receptor LOX-1 promueve la activación y disfunción endotelial al mediar la absorción de LDL oxidada e inducir la señalización pro-aterogénica 41. Se han descrito moduladores de las respuestas mediadas por LOX-1 pero, se sabe poco sobre ellos 42. Se ha descrito la proteólisis como un mecanismo regulador del receptor que se controla a través de su interacción con metaloproteasas (ADAM10) y la degradación lisosómica 43. Los autores consideraron la proteólisis intramembrana por SPPL2a/b como un nuevo mecanismo ateroprotector por medio de la regulación negativa de la señalización de LOX-1.
Por medio de la escisión proteolítica de LOX-1 también se libera la forma soluble de este receptor (sLOX-1) 28, la cual se expresa en la enfermedad cardiovascular 44. Sin embargo, las enzimas proteolíticas responsables de esto han seguido siendo controversiales (43) 45. La función de los fragmentos de escisión individuales y el impacto de la proteólisis en la señalización de LOX-1 no están definidos hasta la fecha.
En cuanto a la expresión de LOX-1, fue reportada por primera vez en células endoteliales de aorta de bovino 15. Se caracterizó como el receptor responsable del reconocimiento, internalización, y degradación de la LDL oxidada. Posteriormente, identificaron LOX-1 en células endoteliales de aorta humana 46.
En el contexto actual conocemos que LOX-1 se expresa principalmente en células endoteliales y también en muchas otras células, incluidas monocitos / macrófagos, células de músculo liso (SMC) 44, cardiomiocitos 47, fibroblastos 48, adipocitos 49, células epiteliales de las vías respiratorias 50, células dendríticas 51 y plaquetas 52. Lo más importante, es que LOX-1 se expresa también en células derivadas de ateroma y se observa en gran abundancia en lesiones ateroescleróticas de animales y humanas 28.
Algunos estudios 33,53,54 han demostrado que la expresión basal de LOX-1 es baja, pero se produce una regulación positiva significativa durante varios estados patológicos que incluyen diabetes, hipertensión y aterosclerosis, debido a la presencia de estímulos inflamatorios y oxidativos y esto provoca un incremento de su expresión 55.
La expresión in vivo de LOX-1 es mucho mayor de que lo que se observa in vitro, es inducida por ciertos activadores proinflamatorios como; Angiotensina II, Factor de necrosis tumoral alfa (TNF- α), Interferón gamma (IFN-γ) entre otros 40. También pueden aumentar su expresión los estímulos oxidativos como la propia LDL oxidada, lisofosfatidilcolina, productos de glicación avanzada 56.
Las tres principales hipótesis de aterosclerosis: modificación oxidativa, respuesta a la lesión y retención; convergieron en las funciones versátiles de LOX-1(Yoshimoto et al., 2011), aumentando su potencialidad como atractiva diana terapéutica.
La evidencia directa de la participación de LOX-1 en la aterogénesis se ha obtenido utilizando modelos animales transgénicos, knock-out de Apolipoproteína E (LOX-1tg / ApoE - / - y transferencia de genes adenovirales 57, 58, 59.
El receptor se encuentra involucrado en una serie de vías de traducción de señales al unirse a una gran variedad de ligandos incluyendo lipoproteínas modificadas, proteína C-reactiva (CRP) y fibronectina. LOX-1 activado está implicado en múltiples vías de transducción de señales que influyen en el inicio y la progresión de la placa de aterosclerosis, Estas vías de señalización incluyen proteínas quinasas activadas por mitógeno (MAP) 60 y se generan especies reactivas de oxígeno (ROS), que estimulan el factor nuclear la vía NF-κB 61. El incremento constante de ROS, debido al proceso inflamatorio, da lugar a la movilización de otras vías de señalización intracelular que impulsan a NF- κB, aumentando aún más la expresión de LOX-1 27. De esta manera, el receptor induce la expresión de moléculas de adhesión y citocinas proinflamatorias y promueve la aterogénesis. También está involucrado en la muerte celular programada (apoptosis) del músculo liso y las células endoteliales; y ejerce una regulación positiva de la actividad caspasa-3 y 9 44. Otra función fisiopatológica de LOX-1, incluye la activación de la enzima arginasa II (ARG2), que conduce a la supresión de los niveles de óxido nítrico (NO) y al aumento del tono vascular 62. Finalmente, LOX-1 está implicada en la disminución de la estabilidad de la placa aterosclerótica a través de una mayor activación de metaloproteasas 63.
Al contribuir en múltiples vías de señalización, LOX-1 se convierte en un objetivo terapéutico potencial. Todo esto conlleva a plantear la posibilidad de considerarlo como un predictor diagnóstico y objetivo terapéutico de la enfermedad cardiovascular.
Un tipo de terapia que se ha estudiado mucho es el beneficio de eliminar LOX-1, que provino del estudio de Hinagata et al. en un modelo de rata de hiperplasia neointimal en una lesión arterial 64. Mehta y col. mostraron más adelante que la deleción del gen LOX-1 se asoció con una disminución del estrés oxidativo, la respuesta inflamatoria, la degradación de NO y la aterosclerosis 65.
Medicamentos como la aspirina 66, los bloqueadores betaadrenérgicos 67 los inhibidores de la reductasa HMG CoA (estatinas) 20 y los bloqueadores del sistema renina-angiotensina (RAS) son fármacos en los que se han evaluado sus efectos con relación a la una posible inhibición de LOX-1 27.
También se ha postulado el uso de sLOX-1 como biomarcador diagnóstico o predictivo de la patología vascular, aunque se necesitan estudios prospectivos y a gran escala para establecer su papel de sLOX-1.68. Los niveles elevados de sLOX-1 están presentes en la hipertensión, diabetes mellitus II; y estos factores de riesgo coexisten en pacientes con enfermedades cardiovasculares, por lo que la interpretación es difícil 69,70.
Existen avances en la fisiopatología de las enfermedades cardiovasculares y la cardiopatía isquémica en las últimas décadas 24. Hasta la fecha no se ha probado ningún tratamiento eficaz de supresión de LOX-1 en humanos.
LOX-1 se continúa investigando como un biomarcador y factor contribuyente a la enfermedad aterosclerótica. Gran parte de las evaluaciones terapéuticas preclínicas de anticuerpos dirigidos contra LOX-1 también se han centrado en esta patología (tabla 1).
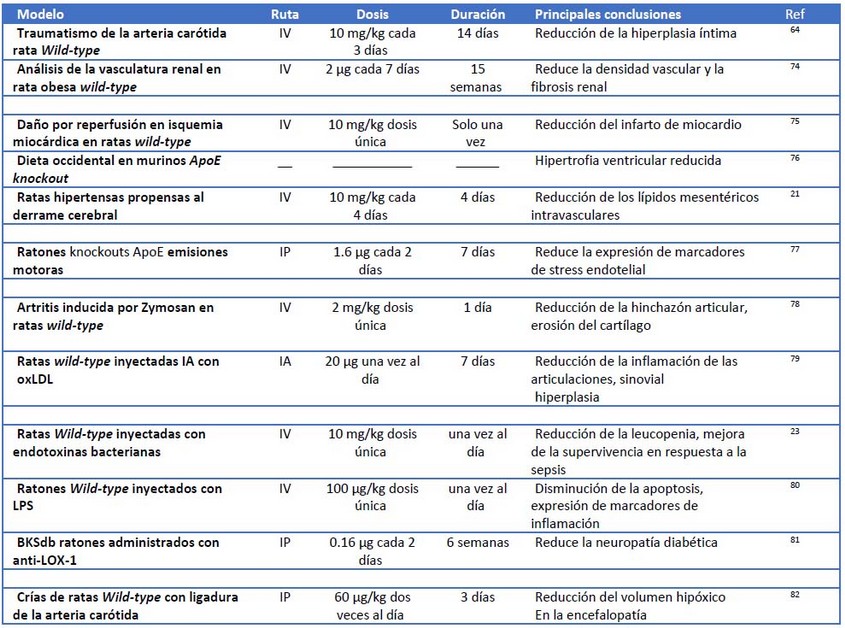
Tabla 1. Evaluaciones terapéuticas preclínicas de anticuerpos dirigidos contra LOX-1
Actualmente, los moduladores sintéticos de LOX-1 se están desarrollando en base a técnicas de interferencia de ARN, diseños de fármacos basados en estructuras y el uso de anticuerpos monoclonales 71,72. En este momento, existen varias estrategias de direccionamiento que inhiben a LOX-1, ya sea mediante el bloqueo directo de la función de la proteína, utilizando anticuerpos monoclonales, o la modulación de la producción, empleando oligonucleótidos anti-sentido 73. Estas investigaciones están en uso clínico, lo que indica que pudieran ser opciones viable para atacar a LOX-1 en humanos 23. No obstante, el desarrollo de anticuerpos monoclonales contra LOX-1 constituye un desafío, debido al dominio de lectina de tipo C altamente conservado de LOX-1 entre las especies de mamíferos 18.
Un ejemplo de esto lo constituye los iPCSK9 54, anticuerpos monoclonales que se unen a la pro-proteína convertasa subtilsina / kexina tipo 9 (PCSK9), importante regulador del metabolismo de las lipoproteínas de baja densidad (LDL), e impiden en parte la degradación de los receptores de LDL y por lo tanto aumentan la expresión de la PCSK9, que regula positivamente la captación de ox-LDL mediada por LOX-1 25.
En resumen, las estrategias de focalización contra LOX-1 en el diagnóstico y tratamiento de la enfermedad aterotrombótica están comenzando a surgir 23. Estas estrategias se encuentran en las primeras etapas de desarrollo y tienen un potencial significativo, pero es necesario descubrir las funciones exactas de LOX-1 para establecer si la selección clínica de este receptor sería efectiva y segura en el futuro.
CONCLUSIONES
La biología y la terapia basada en LOX-1 se han estudiado durante casi 20 años, la evidencia existente indica que LOX-1 es un objetivo potencial para tratar la aterotrombosis mediada por ox-LDL. Algunas enfermedades cardiovasculares, como la hipertensión, la aterosclerosis, el infarto de miocardio, la trombosis y la restenosis coronaria, están mediadas por la activación de LOX-1. La inhibición de LOX-1 por su anticuerpo, análogo químico o transfección de siRNA mejora notablemente las funciones celulares y reduce la probabilidad de formación de lesión aterosclerótica, hipertensión y lesión por isquemia miocárdica, lo que sugiere que atacar LOX-1 se está convirtiendo en una estrategia atractiva para modular la progresión de estas enfermedades cardiovasculares, que pueden traducirse en aplicaciones clínicas.
Financiamiento
REFERENCIAS BIBLIOGRAFICAS
1. oms. Cardiovascular diseases (CVDs). (2017). Available at: https://www.who.int/es/news-room/fact-sheets/detail/cardiovascular-diseases-(cvds). (Accessed: 14th October 2019)
2. Mozaffarian D et al. Heart disease and stroke statistics--2015 update: a report from the American Heart Association. Circulation 131, (2015).
3. Rahman, M. S. & Woollard, K. Atherosclerosis. 121–144 (2017). doi:10.1007/978-3-319-57613-8
4. Kavurma, M. M., Rayner, K. J. & Karunakaran, D. The walking dead: Macrophage inflammation and death in atherosclerosis. Curr. Opin. Lipidol. 28, 91–98 (2017).
5. Yahagi, K. et al. Pathophysiology of native coronary, vein graft, and in-stent atherosclerosis. Nat. Rev. Cardiol. 13, 79–98 (2016).
6. Skålén, K. et al. Subendothelial retention of atherogenic lipoproteins in early atherosclerosis. Nature 417, 750–754 (2002).
7. Yoshida, H., Kondratenko, N., Green, S., Steinberg, D. & Quehenberger, O. Identification of the lectin-like receptor for oxidized low-density lipoprotein in human macrophages and its potential role as a scavenger receptor. Biochem. J. 334, 9–13 (1998).
8. Takei, A., Huang, Y. & Lopes-Virella, M. F. Expression of adhesion molecules by human endothelial cells exposed to oxidized low density lipoprotein. Influences of degree of oxidation and location of oxidized LDL. Atherosclerosis 154, 79–86 (2001).
9. Lubrano, V. & Balzan, S. Roles of LOX-1 in microvascular dysfunction. Microvasc. Res. 105, 132–140 (2016).
10. Baigent, C. et al. Efficacy and safety of cholesterol-lowering treatment: prospective meta-analysis of data from 90 056 participants in 14 randomised trials of statins. Lancet 366, 1267–1278 (2005).
11. Fraley, A. E. & Tsimikas, S. Clinical applications of circulating oxidized low-density lipoprotein biomarkers in cardiovascular disease. Curr. Opin. Lipidol. 17, 502–509 (2006).
12. Winklhofer-Roob, B. M., Faustmann, G. & Roob, J. M. Low-density lipoprotein oxidation biomarkers in human health and disease and effects of bioactive compounds. Free Radical Biology and Medicine (2017). doi:10.1016/j.freeradbiomed.2017.04.345
13. Segrest, J. P., Jones, M. K., De Loof, H. & Dashti, N. Structure of apolipoprotein B-100 in low density lipoproteins. J. Lipid Res. 42, 1346–1367 (2001).
14. Li, D. & Mehta, J. L. Oxidized LDL, a critical factor in atherogenesis. Cardiovascular Research 68, 353–354 (2005).
15. Sawamura, T. et al. An endothelial receptor for oxidized low-density lipoprotein. Nature 386, 73–77 (1997).
16. Shaw, D. J., Seese, R., Ponnambalam, S. & Ajjan, R. The role of lectin-like oxidised low-density lipoprotein receptor-1 in vascular pathology. Diabetes Vasc. Dis. Res. 11, 410–418 (2014).
17. Di Pietro, N., Formoso, G. & Pandolfi, A. Physiology and pathophysiology of oxLDL uptake by vascular wall cells in atherosclerosis. Vascul. Pharmacol. 84, 1–7 (2016).
18. Sugiyama, D. et al. The Relationship between Lectin-Like Oxidized Low-Density Lipoprotein Receptor-1 Ligands Containing Apolipoprotein B and the Cardio-Ankle Vascular Index in Healthy Community Inhabitants: The KOBE Study. J. Atheroscler. Thromb. 22, 499–508 (2015).
19. Aoyama, T. et al. Structure and chromosomal assignment of the human lectin-like oxidized low-density-lipoprotein receptor-1 (LOX-1) gene. Biochem. J. 339, 177–184 (1999).
20. Cheung, B. M. Y., Lauder, I. J., Lau, C.-P. & Kumana, C. R. Meta-analysis of large randomized controlled trials to evaluate the impact of statins on cardiovascular outcomes. Br. J. Clin. Pharmacol. 57, 640–651 (2004).
21. Nishizuka, T. et al. Procyanidins are potent inhibitors of LOX-1: A new player in the French Paradox. Proc. Japan Acad. Ser. B Phys. Biol. Sci. 87, 104–113 (2011).
22. Singh, S. & Gautam, A. S. Upregulated LOX-1 Receptor: Key Player of the Pathogenesis of Atherosclerosis. Curr. Atheroscler. Rep. 21, (2019).
23. De Siqueira, J. et al. Clinical and Preclinical Use of LOX-1-Specific Antibodies in Diagnostics and Therapeutics. J. Cardiovasc. Transl. Res. 8, 458–465 (2015).
24. Jiang, J., Yan, M., Mehta, J. L. & Hu, C. Angiogenesis is a link between atherosclerosis and tumorigenesis: Role of LOX-1. Cardiovasc. Drugs Ther. 25, 461–468 (2011).
25. Ding, Z. et al. PCSK9 regulates expression of scavenger receptors and ox-LDL uptake in macrophages. Cardiovasc. Res. 114, 1145–1153 (2018).
26. Liu, S. & Ding, Z. LOX-1 biology and targeting LOX-1 in cardiovascular diseases. Cardiovasc. Disord. Med. 1, (2016).
27. Kattoor, A. J., Goel, A. & Mehta, J. L. LOX-1: Regulation, Signaling and Its Role in Atherosclerosis. Antioxidants 8, 218 (2019).
28. Kataoka, H. et al. Expression of lectinlike oxidized low-density lipoprotein receptor-1 in human atherosclerotic lesions. Circulation 99, 3110–7 (1999).
29. Kattoor, A. J., Pothineni, N. V. K., Palagiri, D. & Mehta, J. L. Oxidative Stress in Atherosclerosis. (2017). doi:10.1007/s11883-017-0678-6
30. Lü, J. & Mehta, J. L. LOX-1: A critical player in the genesis and progression of myocardial ischemia. Cardiovasc. Drugs Ther. 25, 431–440 (2011).
31. Pothineni, N. V. K. et al. LOX-1 in Atherosclerosis and Myocardial Ischemia: Biology, Genetics, and Modulation. J. Am. Coll. Cardiol. 69, 2759–2768 (2017).
32. Kume, N. & Kita, T. Lectin-like oxidized low-density lipoprotein receptor-1 (LOX-1) in atherogenesis. Trends Cardiovasc. Med. 11, 22–5 (2001).
33. Stancel, N. et al. Interplay between CRP, Atherogenic LDL, And LOX-1 and its potential role in the pathogenesis of atherosclerosis. Clin. Chem. 62, 320–327 (2016).
34. Yamanaka, S., Zhang, X. Y., Miura, K., Kim, S. & Iwao, H. The human gene encoding the lectin-type oxidized LDL receptor (OLR1) is a novel member of the natural killer gene complex with a unique expression profile. Genomics (1998). doi:10.1006/geno.1998.5561
35. Xie, Q. et al. Human Lectin-Like Oxidized Low-Density Lipoprotein Receptor-1 Functions as a Dimer in Living Cells. DNA Cell Biol. 23, 111–117 (2004).
36. Ishigaki, T., Ohki, I., Utsunomiya-Tate, N. & Tate, S. I. Chimeric structural stabilities in the coiled-coil structure of the NECK domain in human lectin-like oxidized low-density lipoprotein receptor 1 (LOX-1). J. Biochem. 141, 855–866 (2007).
37. Xu, S. et al. LOX-1 in atherosclerosis: biological functions and pharmacological modifiers. Cell. Mol. Life Sci. 70, 2859–2872 (2013).
38. Kume, N. & Kita, T. Roles of lectin-like oxidized LDL receptor-1 and its soluble forms in atherogenesis. Curr. Opin. Lipidol. 12, 419–423 (2001).
39. Qian, Y. et al. Site-specific N-glycosylation identification of recombinant human lectin-like oxidized low density lipoprotein receptor-1 (LOX-1). Glycoconj. J. 29, 399–409 (2012).
40. Chen, M., Masaki, T. & Sawamura, T. LOX-1, the receptor for oxidized low-density lipoprotein identified from endothelial cells: Implications in endothelial dysfunction and atherosclerosis. Pharmacology and Therapeutics 95, 89–100 (2002).
41. Akhmedov, A. et al. Endothelial overexpression of LOX-1 increases plaque formation and promotes atherosclerosis in vivo. Eur. Heart J. 35, 2839–2848 (2014).
42. Mentrup, T., Häsler, R., Fluhrer, R., Saftig, P. & Schroder, B. A Cell-Based Assay Reveals Nuclear Translocation of Intracellular Domains Released by SPPL Proteases. Traffic 16, 871–892 (2015).
43. Mentrup, T. et al. Atherogenic LOX-1 signaling is controlled by SPPL2-mediated intramembrane proteolysis. J. Exp. Med. 216, 807–830 (2019).
44. Kataoka, H. et al. Oxidized LDL modulates Bax/Bcl-2 through the lectinlike Ox-LDL receptor-1 in vascular smooth muscle cells. Arterioscler. Thromb. Vasc. Biol. 21, 955–60 (2001).
45. Dong, Y. et al. Activation of protease calpain by oxidized and glycated LDL increases the degradation of endothelial nitric oxide synthase. J. Cell. Mol. Med. 13, 2899–910 (2009).
46. Moriwaki, H. et al. Ligand specificity of LOX-1, a novel endothelial receptor for oxidized low density lipoprotein. Arterioscler. Thromb. Vasc. Biol. 18, 1541–7 (1998).
47. Iwai-Kanai, E. et al. Activation of lectin-like oxidized low-density lipoprotein receptor-1 induces apoptosis in cultured neonatal rat cardiac myocytes. Circulation 104, 2948–2954 (2001).
48. Hu, C. et al. Modulation of angiotensin II-mediated hypertension and cardiac remodeling by lectin-like oxidized low-density lipoprotein receptor-1 deletion. Hypertension 52, 556–562 (2008).
49. Chui, P. C., Guan, H. P., Lehrke, M. & Lazar, M. A. PPARγ regulates adipocyte cholesterol metabolism via oxidized LDL receptor 1. J. Clin. Invest. 115, 2244–2256 (2005).
50. Dieudonné, A. et al. Scavenger receptors in human airway epithelial cells: Role in response to double-stranded RNA. PLoS One 7, (2012).
51. Parlato, S. et al. LOX-1 as a natural IFN-α-mediated signal for apoptotic cell uptake and antigen presentation in dendritic cells. Blood 115, 1554–1563 (2010).
52. Chen, M. et al. Activation-dependent surface expression of LOX-1 in human platelets. Biochem. Biophys. Res. Commun. 282, 153–158 (2001).
53. Hofmann, A., Brunssen, C. & Morawietz, H. Contribution of lectin-like oxidized low-density lipoprotein receptor-1 and LOX-1 modulating compounds to vascular diseases. Vascul. Pharmacol. 107, 1–11 (2018).
54. Ding, Z. et al. Cross-talk between LOX-1 and PCSK9 in vascular tissues. Cardiovasc. Res. 107, 556–67 (2015).
55. Zuniga, F. A. et al. Role of lectin-like oxidized low density lipoprotein-1 in fetoplacental vascular dysfunction in preeclampsia. BioMed Research International 2014, (2014).
56. Oka, K. et al. Lectin-like oxidized low-density lipoprotein receptor 1 mediates phagocytosis of aged/apoptotic cells in endothelial cells. Proc. Natl. Acad. Sci. 95, 9535–9540 (1998).
57. Marwali, M. R. et al. Modulation of ADP-induced platelet activation by aspirin and pravastatin: Role of lectin-like oxidized low-density lipoprotein receptor-1, nitric oxide, oxidative stress, and inside-out integrin signaling. J. Pharmacol. Exp. Ther. 322, 1324–1332 (2007).
58. Hu, C. et al. LOX-1 deletion decreases collagen accumulation in atherosclerotic plaque in low-density lipoprotein receptor knockout mice fed a high-cholesterol diet. Cardiovasc. Res. 79, 287–293 (2008).
59. Inoue, K., Arai, Y., Kurihara, H., Kita, T. & Sawamura, T. Overexpression of lectin-like oxidized low-density lipoprotein receptor-1 induces intramyocardial vasculopathy in apolipoprotein E-null mice. Circ. Res. 97, 176–184 (2005).
60. Wang, R., Ding, G., Liang, W., Chen, C. & Yang, H. Role of LOX-1 and ROS in oxidized low-density lipoprotein induced epithelial-mesenchymal transition of NRK52E. Lipids Health Dis. 9, (2010).
61. Balzan, S. & Lubrano, V. LOX-1 receptor: A potential link in atherosclerosis and cancer. Life Sci. 198, 79–86 (2018).
62. Ryoo, S. et al. OxLDL-dependent activation of arginase II is dependent on the LOX-1 receptor and downstream RhoA signaling. Atherosclerosis 214, 279–287 (2011).
63. Li, D. et al. Expression of lectin-like oxidized low-density lipoprotein receptors during ischemia-reperfusion and its role in determination of apoptosis and left ventricular dysfunction. J. Am. Coll. Cardiol. 41, 1048–1055 (2003).
64. Hinagata, J. I. et al. Oxidized LDL receptor LOX-1 is involved in neointimal hyperplasia after balloon arterial injury in a rat model. Cardiovasc. Res. 69, 263–271 (2006).
65. Mehta, J. L. et al. Deletion of LOX-1 reduces atherogenesis in LDLR knockout mice fed high cholesterol diet. Circ. Res. 100, 1634–1642 (2007).
66. Mehta, J. L., Chen, J., Yu, F. & Li, D. Y. Aspirin inhibits ox-LDL-mediated LOX-1 expression and metalloproteinase-1 in human coronary endothelial cells. Cardiovasc. Res. 64, 243–249 (2004).
67. Li, D. et al. Statins modulate oxidized low-density lipoprotein-mediated adhesion molecule expression in human coronary artery endothelial cells: Role of LOX-1. J. Pharmacol. Exp. Ther. 302, 601–605 (2002).
68. Civelek, S. et al. Soluble Lectin-Like Oxidized LDL Receptor 1 as a Possible Mediator of Endothelial Dysfunction in Patients With Metabolic Syndrome. J. Clin. Lab. Anal. 29, 184–90 (2015).
69. Takanabe-Mori, R. et al. Lectin-like oxidized low-density lipoprotein receptor-1 plays an important role in vascular inflammation in current smokers. J. Atheroscler. Thromb. 20, 585–90 (2013).
70. Yavuzer, S. et al. Endothelial damage in white coat hypertension: role of lectin-like oxidized low-density lipoprotein-1. J. Hum. Hypertens. 29, 92–8 (2015).
71. Yang, X., Wan, M., Cheng, Z., Wang, Z. & Wu, Q. Tofacitinib inhibits ox-LDL-induced adhesion of THP-1 monocytes to endothelial cells. Artif. Cells, Nanomedicine Biotechnol. 47, 2775–2782 (2019).
72. Lekuona, I. PCSK9 Inhibitors: From Innovation to Sustainable Clinical Application. Rev. Esp. Cardiol. 71, 996–998 (2018).
73. Pirillo, A., Norata, G. D. & Catapano, A. L. LOX-1, OxLDL, and atherosclerosis. Mediators Inflamm. 2013, (2013).
74. Dominguez, J. H. et al. Anti-LOX-1 therapy in rats with diabetes and dyslipidemia: Ablation of renal vascular and epithelial manifestations. Am. J. Physiol. - Ren. Physiol. 294, (2008).
75. Li, D. et al. LOX-1 mediates oxidized low-density lipoprotein-induced expression of matrix metalloproteinases in human coronary artery endothelial cells. Circulation 107, 612–7 (2003).
76. Kampschulte, M. et al. Western diet in ApoE-LDLR double-deficient mouse model of atherosclerosis leads to hepatic steatosis, fibrosis, and tumorigenesis. Lab. Investig. 94, 1273–1282 (2014).
77. Lund, A. K. et al. The oxidized low-density lipoprotein receptor mediates vascular effects of inhaled vehicle emissions. Am. J. Respir. Crit. Care Med. 184, 82–91 (2011).
78. Nakagawa, T. et al. Lectin-like oxidized low-density lipoprotein receptor 1 mediates leukocyte infiltration and articular cartilage destruction in rat zymosan-induced arthritis. Arthritis Rheum. 46, 2486–2494 (2002).
79. Rosenbaum, M. A., Miyazaki, K. & Graham, L. M. Hypercholesterolemia and oxidative stress inhibit endothelial cell healing after arterial injury. J. Vasc. Surg. 55, 489–496 (2012).
80. Zhang, B., Ramesh, G., Uematsu, S., Akira, S. & Reeves, W. B. TLR4 signaling mediates inflammation and tissue injury in nephrotoxicity. J. Am. Soc. Nephrol. 19, 923–932 (2008).
81. Schaeffer, D. F. et al. LOX-1 augments oxLDL uptake by lysoPC-stimulated murine macrophages but is not required for oxLDL clearance from plasma. J. Lipid Res. 50, 1676–1684 (2009).
82. Chang, Z. et al. Accelerated atherogenesis in completely ligated common carotid artery of apolipoprotein E-deficient mice. Oncotarget 8, 110289–110299 (2017).
Recibido. 20 febrero 2020
Aceptado: 18 abril 2020
Thelvia I. Ramos Gómez a*, Jorge Roberto Toledo Alonso b
a Departamento Ciencias de la Vida y de la Agricultura, Universidad de las Fuerzas Armadas ESPE, Av. General Rumiñahui s/n, PO BOX 171-5-231B, Sangolquí, Ecuador. ([email protected]) https://orcid.org/0000-0002-0584-6166
*corresponding author: Thelvia I. Ramos [email protected]
b Laboratorio de Biotecnología y Biofármacos, Departamento de Fisiopatología, Facultad de Ciencias Biológicas, Universidad de Concepción, Barrio Universitario s/n, Concepción CP. 4030000, Chile. [email protected]
