2023.08.03.82
Files > Volume 8 > Vol 8 No 3 2023
El 2-Clorobenzilideno Malononitrilo como agente antidisturbios: generalidades y sus efectos en el hombre
2-Chlorobenzylidene Malononitrile as an anti-riot agent: generalities and its effects on the human
Claudia Caballero1 , Lilian Sosa2,3
, Lilian Sosa2,3 , Carlos Puerto Sanabria4
, Carlos Puerto Sanabria4 , Ninoska Alvarenga Arriaga4
, Ninoska Alvarenga Arriaga4 , Valeria Alvarenga Arriaga5
, Valeria Alvarenga Arriaga5 , Claudia Coca6
, Claudia Coca6 , Fredy Rodriguez6*
, Fredy Rodriguez6* 
1 Centro de Información Toxicológico (CENTOX), Facultad de Ciencias Química y Farmacia – Universidad Nacional Autónoma de Honduras. Tegucigalpa, Honduras.
2 Instituto de Investigaciones en Microbiología (IIM), Universidad Nacional Autónoma de Honduras (UNAH), Tegucigalpa, Honduras.
3 Instituto de Investigaciones en Ciencias Tecnológicas y Aplicadas (IICAT), Universidad Nacional Autónoma de Honduras (UNAH), Tegucigalpa, Honduras.
4 Medicina Legal y Forense, Instituto Hondureño de Seguridad Social IHSS. Tegucigalpa, Honduras.
5 Facultad de Ciencias Medicas – Universidad Nacional Autónoma de Honduras. Tegucigalpa, Honduras.
6 Departamento de Química, Facultad de Ciencias Química y Farmacia – Universidad Nacional Autónoma de Honduras. Tegucigalpa, Honduras.
* Autor Correspondiente. [email protected]
Available from: http://dx.doi.org/10.21931/RB/2023.08.03.82
RESUMEN
El 2-Clorobenzilideno Malononitrilo o CS es uno de los componentes presentes en los gases lacrimógenos utilizados en Honduras. En el presente artículo, nos enfocamos en una revisión general de lo que es el compuesto CS, sus características químicas, toxicocinéticas y toxicodinámicas. Así como el manejo de personas afectadas y métodos de análisis para la detección de este. El CS puede causar efectos adversos leves como lagrimeo hasta mortales como hepatotoxicidad. Es importante que la población conozca los efectos que causa el CS en el organismo, en especial aquellas personas que trabajan en contacto con esta sustancia. Es importante prevenir el contacto con gases lacrimógenos.
Palabras claves: Bombas lacrimógenas, gases tóxicos, 2-Clorobenzilideno Malononitrilo, toxicocinética, toxicodinamia.
ABSTRACT
2-Chlorobenzylidene Malononitrile, or CS, is one of the components present in the tear gas used in Honduras. In this article, we focus on a general review of the CS compound and its chemical, toxicokinetic and toxicodynamic characteristics. As well as the management of affected people and analysis methods for its detection. CS can cause mild adverse effects such as lacrimation to fatal ones such as hepatotoxicity. The population must know CS's impact on the body, especially those working with this substance. It is essential to prevent contact with tear gas.
Keywords: Tear gas bombs, toxic gases, 2-chlorobenzylidene Malononitrile, toxicokinetics, toxicodynamics.
INTRODUCCIÓN
En el siglo XXI, los cambios sociopolíticos han marcado la historia con hechos violentos que alteran el orden social y obligan a las instituciones de seguridad pública a buscar mecanismos disuasivos menos letales a fin de restablecer el orden, de igual forma, estos medios son utilizados para someter a criminales que se encuentran atrincherados1.
El uso de los gases irritantes no es una medida nueva cuando se trata de establecer el orden y someter a grandes grupos ya que su uso se remonta en el siglo XX durante la primera Guerra Mundial, donde se desarrollaron gases neumotóxicos y vesicantes durante la contienda bélica a pesar de que el uso de “gases asfixiantes y deletéreos” estaba prohibido por la Conferencia Internacional de Paz de La Haya de 1899 y la posterior Convención de La Haya de 1907. Los franceses fueron los primeros en usar gases neumotóxicos, al utilizar bromoacetato de etilo, una sustancia lacrimógena, para forzar a las tropas alemanas a salir de sus búnkeres en 1914, aunque su efecto era prácticamente nulo, al emplearse al aire libre. Posterior a ello, entró en acción el ejército alemán al quedarse sin el suministro de los nitratos chilenos para la fabricación de pólvora y explosivos por el bloqueo marítimo británico. Es por lo anterior que el Departamento de Materias Primas del Ministerio de la Guerra enroló al científico Fritz Haber, en aquel momento director del Instituto Kaiser Wilhelm de Física, Química y Electroquímica de Berlín, y premio nobel de química para solucionar el problema. Es por esto que en su laboratorio desarrollaron las primeras armas de destrucción masiva conocidas, como una alternativa. El primer gas utilizado fue el clorosulfonato de o-dianisidina, sin apenas eficacia, y posteriormente el cloro, ensayado contra las tropas francesas en el año 1915. Luego se fueron sintetizando nuevos compuestos hasta que, al finalizar la primera guerra mundial, Fritz sintetizó el amoniaco, un gran descubrimiento para la ciencia, pero a la vez paradójico ya que este compuesto provocó miles de muertes. A pesar de la cantidad de víctimas resultado del descubrimiento de sustancias tóxicas, en el discurso leído durante la ceremonia de entrega del Premio Nobel, Fritz el “padre de la guerra química” dijo: “En ninguna guerra venidera los militares podrán ignorar los gases tóxicos. Son una forma superior de matar”1.

Figura 1. Fritz Haber, padre de la guerra química1
Dentro del grupo de gases los gases tóxicos se encuentran el 2-clorobenzilideno malononitrilo (CS) el cual es un agente químico irritante muy conocido como componente del gas lacrimógeno y hoy en día es el más utilizado por su margen de seguridad y baja toxicidad. Su nomenclatura proviene de sus creadores, fue descubierto y desarrollado en la década de 1920 por Ben Corson y Roger Stoughton2, y desde 1950 es usado en el control de manifestaciones civiles en muchos países alrededor del mundo3; a nivel mundial, países bajos, Bélgica y la República Eslovaca prohíben el uso del gas lacrimógeno, específicamente por el contenido de CS en estos4. No obstante, en Honduras el uso de gases lacrimógenos no es prohibido y en esta revisión científica, se indagará los antecedentes del uso de estos en Honduras en diferentes contextos y su toxicidad.
Uso de gas lacrimogeno en Honduras
Los registros en Honduras con relación al uso del gas lacrimógeno por parte de las autoridades responsables de la seguridad pública, se puede rastrear desde finales del siglo XX, sin embargo desde el conflicto político de 20095 hasta el más reciente llevado a cabo durante el periodo 2017-2018 relacionado a las elecciones y toma de posesión en Honduras, se reportó el uso de gas lacrimógeno por parte de la Policía Nacional (Figura 1) lo que ha generado debates entorno a su efectividad, seguridad y legalidad en relación al cumplimiento de la normativa y estándares internacionales referente a los derechos humanos6, sin embardo, se ha podido identificar algunas referencias sobre las bases legales que le permiten a las instituciones responsables de mantener el orden y la seguridad a nivel nacional el uso de este tipo de dispositivos. Es así que para este fin debemos considerar que Honduras ha suscrito convenios internacionales que le obligan a regular las acciones de estas instituciones en el marco del respeto a los derechos Humanos, como son: la Convención sobre Armas Químicas7 y el Manual de uso de la fuerza y armas de fuego de la Policía Nacional de Honduras el cual posee lineamientos específicos para el uso de armas menos letales como medios disuasivos para el control de disturbios8.

Figura 2. Dina Meza “Honduras: Gases, uso excesivo de la fuerza y detenciones en el primero de mayo”, Pasos de animal Grande, 2018. En la foto las bombas lacrimógenas lanzadas, fueron decenas usadas para reprimir a los manifestantes8.
Según la prensa nacional, la secretaria en el Despacho de Seguridad de Honduras durante el periodo 2017 al 2021 hizo una adquisición de 157,000 municiones de gases lacrimógenos en diferentes presentaciones, siendo las más comunes las granadas de gas para escopeta y la granada de gas para mano trifásicas9. Esto sugiere un incremento estratégico en la adquisición de estos agentes por parte de las autoridades, lo cual permite facilitar la disponibilidad haciendo cada vez más común el empleo de los mismos. El principal motivo por el cual se ha incrementado su uso en el país es porque se tiene la percepción que es un método más seguro para el control de disturbios, sin embargo, en las presentaciones antes descritas ya no se puede referir a ellas como armas no letales, sino que entran en la categoría de armas menos letales debido a que si bien es cierto no están diseñadas para ser letales existe la posibilidad que en determinadas circunstancias si lo sean.
Organismos internacionales han investigado los abusos en el uso de estos dispositivos llegando a la conclusión que no solo se deben considerar las afectaciones inmediatas del principio activo principal, sino también los riesgos que representan para la salud los demás componentes que forman parte del mismo10. Al revisar las especificaciones de este tipo de dispositivos se puede obtener una información sobre su formulación y se sabe que su componente principal es el 2-clorobenzilideno malononitrilo (CS)11-15.
Debido a que el uso de bombas de gas lacrimógeno se ha vuelto cada vez más común hace que desde la perspectiva de la toxicología esta práctica deba ser vigilada y documentada. a fin de establecer claramente cuál es la composición química. Asimismo, dar a conocer a la población cuáles son los efectos causados por la exposición a los diferentes agentes tóxicos que forman parte de su composición, siendo esto importante ya que permitiría identificar si existe una relación entre las atenciones en las salas de emergencias y la exposición al mismo, o en los casos que su exposición ha resultado letal determinar exactamente cuál de los agentes es realmente el responsable de ese resultado ya que los mecanismos de toxicidad de estos agentes son tan variados se deben considerar únicamente los más relevantes o los que se encuentran en mayor concentración en la formulación.
Composicion quimica de las municiones de gas lacrimogeno usadas en Honduras
Desde el punto de vista de la química se sugiere que puedan existir diferentes formulaciones para estos dispositivos, sobre los cuales comúnmente se hace referencia a ellos como “bombas de gas lacrimógeno”, realmente sus componentes no se encuentran en estado gaseoso esto debido a la naturaleza química de los mismos es así que de acuerdo a su uso podemos ver presentaciones diferentes entre las cuales están: Los aerosoles comúnmente usados para defensa personal (uso civil) y la presentación de granadas o botes para uso táctico (uso militar). En el caso de los aerosoles estos usan una formulación líquida que se entrega gracias a un dispensador presurizado, mientras que las granadas usan una forma solida donde se mezcla el principio activo el cual es sólido con una mezcla pirotécnica que se puede dispersar como humo o niebla.
Considerando el tipo de dispositivo que utiliza la policía a nivel nacional y los proveedores de este tipo de munición9, se puede describir cual es la composición química de la munición utilizada en Honduras, la cual se detalla a continuación:
1. Para las granadas de gas para mano trifásica modelo MP-3-CS el fabricante indica que el dispositivo consta de 3 submuniciones (Figura 2) que se liberan separadas en la descarga después del lanzamiento, que posee aproximadamente 240g de sustancias químicas de las cuales 65g corresponden al peso neto del agente irritante CS11.
Según la ficha técnica se indica que la composición química corresponde a una mezcla de un 25% - 40% de CS, 25% - 40% de Clorato de Potasio, 10% - 20% de Carbonato de Magnesio, 10% - 20% de Sacarosa pura, <5% de Nitrato de Potasio, <5% de Nitrocelulosa coloidal, , <2% de Silicon y , <1% de Tiocianato de Plomo II12.
Es así que para las granadas para escopeta, se encuentran disponibles al menos 2 modelos MP-4L-CS 37mm-38mm13 y el modelo Skat Shell® 37 mm CS (Figura 4) estos dispositivos entregan submuniciones una vez que se descarga, logrando alcanzar así aproximadamente 100 yds.
Según la ficha técnica para el modelo MP-4L-CS se indica que la composición química corresponde a una mezcla que contiene los siguientes componentes: CS, oxido de magnesio, carbonato de magnesio, perclorato de potasio, cromato de bario , polvo de aluminio metálico en polvo, níquel, polvo de zirconio, 2,4,6-trinitro-m-fenilendioxido de plomo14.
Según la ficha técnica para este modelo se indica que la composición química corresponde a una mezcla que contienen los siguientes componentes: CS , nitrocelulosa granular, nitroglicerina, nitrato de potasio, perclorato de potasio, difenilamina,1,3-dietildifenilurea, oxido de magnesio, silica amorfa, hierro, cobre, oxido de zirconio, nitrato de bario, 2,4,6-trinitro-m-fenilendioxido de plomo, tiocianato de plomo II 15.
Como se observa todas las municiones contienen CS, siendo este el principio activo principal como agente lacrimógeno embargo como se mencionó anteriormente las formulaciones están dadas de acuerdo al tipo de dispositivo, es por eso que en Honduras las municiones tipo granadas es la presentación más común, haciendo necesario considerar los riesgos que este tipo de presentación representa debido a los componentes de las mezclas pirotécnicas que permiten la difusión del CS después de una combustión donde estos componentes también son liberados elevando el riesgo de quienes se exponen a estos humos.
Dentro de estas mezclas pirotécnicas se han identificado como componentes más comunes los siguientes: Perclorato de potasio, níquel, sales de plomo como ser 2,4,6-trinitro-m-fenilendioxido de plomo, tiocianato de plomo II (ver tabla 1), su identificación se hace interesantya que, debido a su concentración, características y grado de toxicidad su estudio también se vuelve significativo debido a que mezclas son las responsables de la variedad de efectos sobre la salud de quienes manipulan y se exponen a sus gases16.
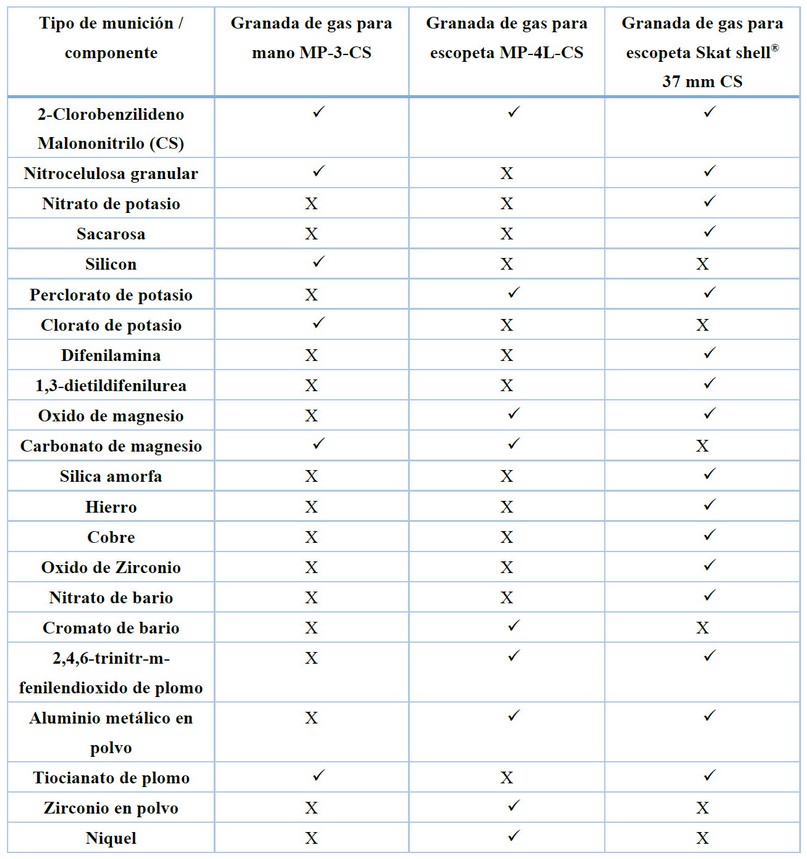
Tabla 1. Cuadro comparativo entre la composición de los diferentes tipos de municiones16.
Si bien es cierto que para poder definir de manera amplia los efectos toxicológicos de las municiones de Gas lacrimógeno es necesario conocer las características individuales de cada uno de los compuestos antes mencionados, en este apartado el enfoque principal será el definir las características fisicoquímicas del CS, sin embargo, más adelante se tomarán en cuenta los efectos tóxicos más relevantes de estos compuestos a fin de valorar los riesgos asociados a la exposición de estas mezclas pirotécnicas .
Propiedades fisicas y quimicas de el 2-clorobenzilideno malononitrilo (cs)
El CS conocido también como O-Clorobenzilideno Malononitrilo su N° CAS es 2698-41-1, posee una formula molecular de ClC6H4CH=C(CN)2. Estructuralmente, la molécula de CS posee un átomo de cloro en α de una función activadora, el Bencilideno Malonitrilo, que es característico de muchas moléculas con actividad lacrimógena. Esta actividad se puede ver potenciada cuando se coloca la molécula de CS en presencia de Agua, ya que libera 2- Clorobenzaldehído, cuya estructura contiene también un átomo de cloro en α de Función Aldehído, el cual es también conocido por sus propiedades lacrimógenas17.
El CS posee las siguientes propiedades físicas: punto de ebullición de alrededor de 350°C. Esto indica que se descompone y vaporiza a altas temperaturas, su punto de fusión es de alrededor de 93°C, lo que indica que es un sólido a temperatura ambiente. Sin embargo, puede sublimar cuando se calienta, es soluble en disolventes orgánicos polares como el alcohol y la acetona, pero es prácticamente insoluble en agua. Esta baja solubilidad en agua contribuye a su persistencia y eficacia como agente lacrimógeno. Con respecto al color y apariencia, El CS puro es un sólido cristalino que varía de blanco a amarillo pálido. En forma de aerosol, se dispersa en una densa niebla blanca18.
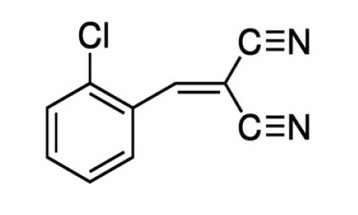
Figura 3. Estructura química del CS
En relación a sus propiedades químicas y especialmente refiriéndose a su reactividad se puede decir que el CS es relativamente estable y no inflamable en condiciones normales. Sin embargo, puede reaccionar con sustancias alcalinas fuertes o agentes reductores, dando como resultado la formación de compuestos tóxicos o inflamables19.
El CS puede sufrir descomposición térmica a altas temperaturas, generando gases tóxicos. La descomposición produce compuestos como el cloruro de hidrógeno (HCl) y el cianuro de hidrógeno (HCN), que representan un riesgo adicional para la salud y la seguridad, se considera un compuesto persistente, lo que significa que puede permanecer en el medio ambiente durante un período prolongado de tiempo después de la dispersión. Esta característica se debe a su baja volatilidad y baja solubilidad en agua. La persistencia de CS puede provocar efectos a largo plazo y dificultar la limpieza de las áreas afectadas17-19.
Mecanismos de toxicidad
Toxicocinética
La absorción del CS puede llevarse a cabo mediante la piel. Al ser el CS un compuesto liposoluble, se absorbe rápidamente por la epidermis que al igual es la parte más liposoluble de la piel generando dermatitis por contacto, incluso después de lo que pudiese parecer una exposición inicial sin efectos inmediatos, desarrollando severas ampollas, aun horas más tarde20.
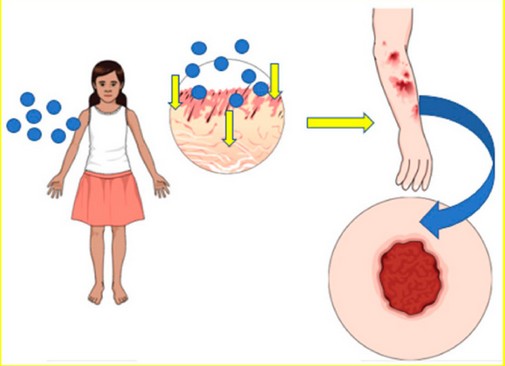
Figura 4. Absorción de CS a través de la piel. Fuente: elaboración propia.
La absorción del CS es rápida cuando se inhala, el cual entra en contacto con el torrente circulatorio al unirse con las proteínas plasmáticas para formar compuestos de naturaleza extraña al organismo, conocida comúnmente como antígeno y generando hipertensión arterial y falla cardíaca21,22.
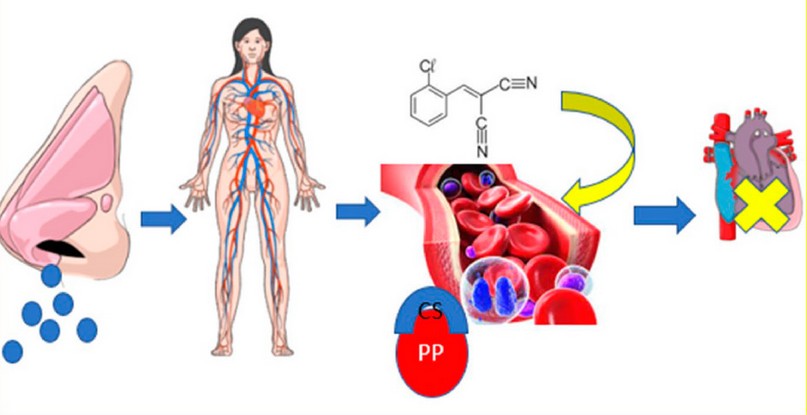
Figura 5. Absorción del CS por vía respiratoria y unión a proteínas plasmáticas. Fuente: elaboración propia.
Al intentar metabolizarse en el hígado, el CS se hidroliza en dos compuestos: clorobenzaldehido y malononitrilo, este último se transforma en cianuro en los tejidos animales, por su parte el clorobenzaldehido se metaboliza en mayor cantidad como ácido Clorohipúrico y en menor cantidad ácido Clorobenzoico generando daño hepático y muerte22.
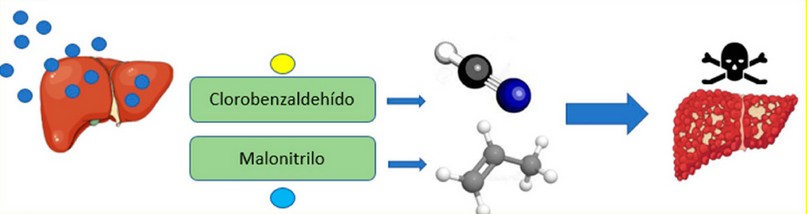
Figura 6. Metabolismo del CS y productos de hidrolisis. Fuente: elaboración propia.
Toxicodinámica
Los mecanismos de toxicidad del CS son variados, por lo que podríamos considerar los más relevantes según la literatura:
a. Activación de receptores de potencial transitorio (TRP) de fibras nerviosas sensoriales.
b. Inactivación de enzimas (CS actúa como alquilante) que conlleva a daño tisular.
c. Liberación de bradiquininas, produciendo irritación y dolor.
Los TRP incluyen una gran familia de seis tipos: TRPC, C para “canónico”; TRPA, A para “anquirina”; TRPM, M para “melastatina”; TRPML, ML para “mucolipidina”; TRPP, P para “policistina”; y TRPV, V para “vaniloide”. Se consideran sensores celulares del entorno en que nos desenvolvemos, ubicados en casi todas las células del organismo. Están involucrados en la termo sensación, nocicepción, así como en la percepción mecánica, química, osmolar y del gusto. Al recibir estímulos, son capaces de transmitir señales que terminan evocando una respuesta. Al estimular estos canales, la membrana celular se vuelve permeable a cationes (calcio, sodio y potasio) que lleva a la despolarización de la misma, activando mecanismos de señalización que llevan a la liberación de neuropéptidos (sustancia P, neuroquinina A)23--29. Un exceso de sustancia P puede conllevar a taquicardia, temblor, sudoración, crisis epilépticas y alucinaciones visuales, táctiles y auditivas. Por otro lado, la neuroquinina A actúa como neurotransmisor, tanto en nervios periféricos como en el sistema nervioso central, y es de particular interés en la transmisión de la sensación dolorosa y en procesos inflamatorios. Particularmente, en el caso del CS, se sospecha que activa el receptor TRPA1 (anteriormente llamado ANKTM1) el cual se transduce en señales inflamatorias mecánicas, térmicas, relacionadas con el dolor, irritación de los ojos, lo que provoca lágrimas excesivas y calambres en los párpados (blefaroespasmo) que es precisamente lo que sucede al estar en contacto con gases lacrimógenos30,31[Rev 12] .
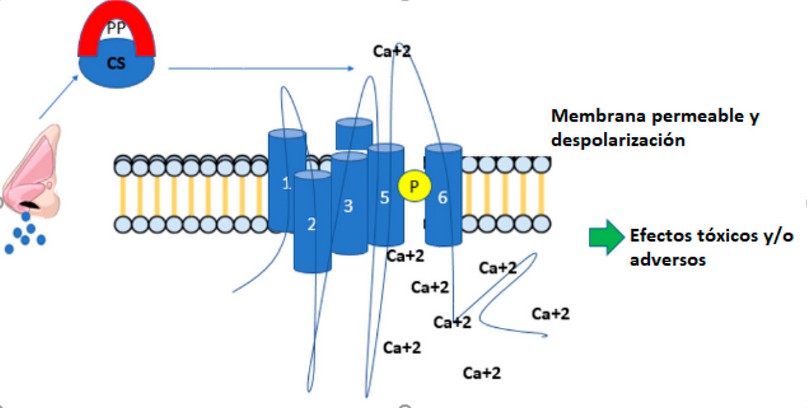
Figura 7. Probable mecanismo de acción del CS en el organismo de los mamíferos. Fuente: elaboración propia.
Manifestaciones clínicas
Anteriormente se han mencionado algunos de los signos y síntomas que puede ocasionar el efecto del CS en los seres humanos. A continuación, resumimos las diversas manifestaciones clínicas que se han reportado en la literatura debido a la exposición de gases lacrimógenos:
En ojo: uno de los órganos principalmente afectados son los ojos. Dentro de las manifestaciones clínicas tenemos: lagrimeo, blefaroespasmo, prurito, sensación quemante, ojo rojo, fotofobia, inyección difusa conjuntival y edema estromal de la córnea. En mayor gravedad presenta desgarro conjuntival, hemorragia vítrea, neuropatía traumática del nervio óptico, simblefaron, queratitis infecciosa o necrosante, queratoplastia trófica, glaucoma, catarata y erosión corneal hasta ocasionar la pérdida de visión24, 32-34.
En piel: enrojecimiento, sensación quemante, quemadura, prurito, abrasión, vesículas, descamación, dermatitis por contacto y edema21, 32-36.
El aparato respiratorio: tiende a ser uno de los más afectados, viéndose manifestado en individuos que trabajan en fábricas productoras de dichas sustancias o integrantes de la milicia en quienes se realizan pruebas o entrenamientos exponiéndolos a estos químicos. En su mayoría, con estas exposiciones se llega a provocar: irritación de membranas mucosas, rinorrea, estornudos, tos, hemoptisis, sensación quemante a nivel de faringe, laringoespasmo, opresión torácica, ruidos respiratorios como ser sibilancias, derrame pleural y asma. Cabe resaltar que dicha exposición puede dar lugar a infecciones tales como nasofaringitis, sinusitis, bronquitis y neumonitis química y en el peor de los casos inducir una falla respiratoria pudiendo terminar en la muerte32,33,34,37,38.
En el sistema gastrointestinal: la persona expuesta rara vez manifiesta sintomatología de este tipo, pudiéndose presentar salivación, dolor abdominal, retortijones, nausea, vomito, diarrea e incluso hematemesis24,33,34,36.
En cuanto a los síntomas agudos: dolor tipo urente en ojos, lagrimeo excesivo, junto con ojo rojo; sensación quemante en vía área, cavidad oral y piel; rinorrea y tos, odinofagia, rash, quemaduras, cefalea, desorientación y mareos. Así mismo, alteración de la conciencia pudiendo manifestarse en ansiedad, respuesta sobresaltada, miedo, fatiga, tristeza o depresión34.
En cuanto a los síntomas crónicos: Irritación nasal, disnea, odinofagia, raramente paro respiratorio, sibilancias, opresión torácica o cambios en el patrón respiratorio. Se menciona que crónicamente existe la posibilidad de encontrar secuelas tales como asma, bronquitis crónica, bronquiectasia y fibrosis pulmonar. Los efectos respiratorios pueden perdurar tras la exposición por un periodo aproximado de 10 meses, persistiendo como tos, o alterando la tolerancia al realizar actividad física y si el individuo tiene alguna comorbilidad, exacerbándola38,39.
Manejo
El personal médico portando la vestimenta adecuada (mascarilla quirúrgica, guantes y trajes que abarquen la mayor superficie corporal) deberá movilizar la víctima lejos del área contaminada hacia un área con adecuada ventilación. Así mismo, deberá retirar toda prenda que porte la víctima por medio del corte de las mismas y posteriormente descartar en bolsas selladas herméticamente. Luego, el personal médico procederá a realizar la evaluación primaria de la víctima en base al ABCDE (airway, breathing, circulation, disability y exposure).
Dependiendo del área afectada será: a nivel ocular se proseguirá a realizar una irrigación profusa por más de 10 minutos haciendo uso de solución isotónica como ser solución salina al 0.9% y si porta lentes de contacto, retirarlos. Cuando el gas lacrimógeno entra en contacto con la piel, la mayor parte de expertos sugiere si el compromiso es de mayor gravedad se complementa con el uso de antihistamínicos y esteroides. Para tratar los síntomas respiratorios, se recomienda la aplicación de aerosoles de Ipatropio, B2 miméticos u oxigenoterapia suplementaria. Si en dado caso el individuo presenta síntomas gastrointestinales, puede ser adecuado el suministro de líquidos endovenosos y/o antieméticos, ya que este tipo de manifestaciones son poco comunes y autolimitadas. Si cualquiera de los síntomas persiste, se deberá referir al especialista y según la gravedad de la afectación se decidirá el ingreso hospitalario40,41.
Estudios postmortem
En casos de muertes relacionadas a gases lacrimógenos, es mandatorio el estudio del caso mediante autopsia médico legal. En vista que en estas muertes existe sospecha de haber sido causadas por actos u omisiones del estado, de sus órganos o agentes, o puede ser atribuible al estado, en violación de su obligación de respetar el derecho a la vida, la autopsia debe realizarse siguiendo los lineamientos dictados en el Protocolo de Minnesota42,43.
La exposición a CS tiene un efecto irritante en las membranas de las mucosas, causando neumonitis química y edema pulmonar. Al examen histológico, la irritación de las mucosas se puede manifestar como traqueobronquitis, necrosis aguda superficial de la mucosa, infiltrado celular inflamatorio, descamación epitelial, bronconeumonía y membranas hialinas. El edema pulmonar se acompaña de hemorragia intraalveolar, en especial en las áreas postero-basales35,37.
Asimismo, se han publicado casos donde la muerte es ocasionada por traumas craneoencefálicos ocasionados por el proyectil del frasco donde se contienen estos gases44.
Metabolitos o biomarcadores de interés analítico
Después de la rápida absorción del CS por las vías respiratorias, tanto el compuesto como sus principales metabolitos tienen una vida media extremadamente corta. El CS se hidroliza de forma espontánea a malononitrilo, el cual se transforma rápidamente en cianuro en los tejidos animales45-47. El CS experimenta una serie de transformaciones metabólicas en el organismo humano después de la inhalación de altas concentraciones, estas transformaciones incluyen la formación de varios metabolitos como el 2-Clorobencilmalononitrilo, 2-Clorobenzaldehido, acido 2-Clorohipurico y tiosulfato. Tanto el CS como como sus metabolitos pueden ser detectados en sangre después de la inhalación de altas concentraciones; estos compuestos pueden ser medidos mediante técnicas analíticas sensibles como la cromatografía de gases acoplado a espectrometría de masas48.
Estudios realizados en especies roedores y no roedores se detectaron CS y dos de sus metabolitos, específicamente el 2-Clorobenzaldehido y 2-Clorobencilmalononitrilo luego de que las especies fueron expuestas a altas concentraciones49. Se ha evidenciado que luego de la adsorción de CS en seres humanos por el tracto respiratorio a altas concentraciones, se ha detectado en cantidades mínima en sangre del metabolito 2-Clorobencilmalononitrilo50. Asimismo, en un trabajo se llevó a cabo la determinación de diferentes metabolitos del CS, entre ellos, el tiocianato en seres humanos expuestos a altas concentraciones consideradas intolerables, algunos de ellos eran fumadores y otros no. Se midieron los niveles de tiocianato en orina y plasma, antes y después de la exposición al CS, por lo que se procedió a comparar las concentraciones del tiocianato en voluntarios fumadores obstinados, fumadores ocasionales y no fumadores , demostrando que no hubo diferencia estadística en la concentración de tiocianato en plasma y orina entre voluntarios expuestos y no expuesto a CS, aunque si, un poco más elevados los niveles de tiocianato en los individuos fumadores que en los no fumadores, esto debido a que al fumar cigarrillos también aumenta la concentración de tiocianato en fluidos corporales de personas fumadoras 22 .
Los gases lacrimógenos son utilizados como medidas disuasivas para reestablecer el orden en procesos de huelgas, manifestaciones y cualquier disturbio que altere el orden público. Este tipo de sustancias son utilizados desde hace más de un siglo, no obstante, aunque se considere que el uso es legal, es importante determinar el tipo de compuestos y los efectos adversos y tóxicos que estos generan para los seres humanos y animales. En Honduras, los gases lacrimógenos utilizados están compuestos por 2-Clorobenzilideno Malononitrilo o CS el cual puede provocar daños en ojos, piel y tejidos y en dependencia de la exposición al mismo, efectos como hepatotoxicidad, bronquitis crónica, bronquiectasia y fibrosis pulmonar pudiendo provocar la muerte de las víctimas. Más estudios son necesarios realizar, específicamente en aquellos casos donde se sospecha de la intoxicación por CS.
Agradecimientos: agradecemos a la Dirección de Investigación Científica, Humanistica y Tecnológica (DICIHT) por el apoyo brindado para la escritura y revision de este manuscrito.
Conflicts of Interest: Los autores declaran no tener conflictos de interes.
Todos los autoreshan leído el manuscrito y están de acuerdo para su publicación.
REFERENCIAS
1. Tragedia de los gases de la muerte durante la gran guerra. Available from: https://historia.nationalgeographic.com.es/a/tragedia-gases-muerte-durante-gran-guerra_15712 (accessed on 4 de septiembre de 2023).
2. Blain, P.G. Tear Gases and Irritant Incapacitants. Toxicol Rev. 2003, 22(2), 103–10.
3. Hu, H.; Fine, J.; Epstein, P.; Reynolds, P.; Walker, B. Tear Gas-- Harassing Agent or Toxic Chemical Weapon ?. JAMA, 1989, 262(5), 660.
4. Usos de gases lacrimogenos, normativa nacional, extrangera e internacional . Available from: https://obtienearchivo.bcn.cl/obtienearchivo?id=repositorio/10221/27512/1/BCN_GF_Uso_de_gases_lacrimogenos_FINAL.pdf (accessed on 2 de julio 2023).
5. Intervención de la UDUAL y Organismos internacionales ante conflictos violentos en la Universidad Nacional Autónoma de Honduras. 2009. Universidad Nacional Autónoma de Honduras. 2009. Available from: http://dspaceudual.org/handle/Rep-UDUAL/314 (accessed on 2 de julio 2023)
6. Hernández Alegría, R.A.; Hernández Arias, M.L.; Torres Vasco, M.C.; Palao Varela, K.R.; Contreras, M.I. LXII CONGRESO MÉDICO NACIONAL: Dr. Andres Castillo Amaya . Rev Med Hondur. 2019, 87(Supl.1):S1–106.
7. Bothe, P.M. Convención sobre la prohibición del desarrollo, la producción, el almacenamiento y el empleo de armas químicas y sobre su destrucción. Available from: www.un.org/law/avl (accessed on 2 de julio 2023)
8. Manual de uso de la fuerza y armas de fuego de la Policía Nacional de Honduras. 2023;33–40. Available from: https://www.dcaf.ch/sites/default/files/imce/LAC/MANUAL-USO-FUERZA-ARMAS-FUEGO-PNH.pdf (accessed on 2 de julio 2023)
9. No hay documentos de respaldo en la compra de 117 mil bombas lacrimógenas. Available from: https://www.elheraldo.hn/elheraldoplus/investigaciones/documentos-bombas-lacrimogenas-compras-IH13509405 (accessed on 2 de julio 2023)
10. Gas Lacrimógeno: Investigación – Amnesty International. Available from: https://teargas.amnesty.org/es/#top (accessed 2 de julio 2023)
11. NonLethal Technologies, Inc, Especificación técnica MP-3-CS. 2019. Available from: https://www.nonlethaltechnologies.com/pdf/DS/MP-3-CS.pdf (accessed 2 de julio 2023)
12. NonLethal Technologies, Inc, Ficha de seguridad MP-3-CS. 2019. 2019. Available from: https://www.nonlethaltechnologies.com/pdf/DS/MP-3-CS.pdf (accessed 2 julio 2023)
13. NonLethal Technologies, Inc, Especificación técnica MP-4L-CS. 2016. Available from: https://www.nonlethaltechnologies.com/pdf/DS/MP-4L-CS.pdf (accessed 2 de julio 2023)
14. NonLethal Technologies, Inc, ficha de seguridad MP-4L-CS. 2016. Available from: https://www.nonlethaltechnologies.com/pdf/DS/MP-4L-CS.pdf (accessed 2 de julio 2023)
15. Defense Technology, Inc, ficha de seguridad Skat Shell® 37 mm CS. 2015. available from: https://www.nonlethaltechnologies.com/pdf/DS/MP-4L-CS.pdf (accessed 2 de julio 2023)
16. Rothenberg, C.; Achanta, S.; Svendsen, E.R.; Jordt, S. Tear gas: an epidemiological and mechanistic reassessment. Ann N Y Acad Sci. 2016, 1378(1), 96–107.
17. Samuel, A.; Picot, A. L’utilisation du gaz lacrymogene CS ses effects toxiques a plus ou moins long terme. 2020, 1–127.
18. Olajos, E.J.; Salem, H. Riot control agents: pharmacology, toxicology, biochemistry and chemistry. J Appl Toxicol. 2001, 21(5), 355–91.
19. Horowitz, B.Z.; Tear gas in America: Cry the Beloved Country. Toxicol Commun. 2020, 4(1), 59–61.
20. Crowd Control Technologies. Available from: https://www.europarl.europa.eu/RegData/etudes/etudes/stoa/2000/168394/DG-4-STOA_ET(2000)168394_EN(PAR02).pdf (accessed 2 de septirmbre de 2023)
21. Lukey, B.J.; Romano, J.; Romano, J.A.; Salem,H.; Lukey, B.J. Chemical Warfare Agents: Chemistry, Pharmacology, Toxicology, and Therapeutics, Second Edition. 2nd, ilustra ed. Press 5. CRC, editor. 2007. 752 p.
22. Danforth, J.C. Possible lethal effects of CS tear gas on Branch Davidians during the FBI raid on the Mount Carmel compound near Waco , Texas The Office of Special Counsel. 2000. Available from: http://www.veritagiustizia.it/docs/gas_cs/CS_Effects_Waco.pdf (accessed on 4 de septiembre 2023)
23. Dietrich, A. Transient receptor potential (TRP) channels in health and disease. Cells. 2019;8(5).
24. Rothenberg, C.; Achanta, S.; Svendsen, E.R.; Jordt, S.E. Tear gas: an epidemiological and mechanistic reassessment. Ann N Y Acad Sci. 2016. 1378(1), 96–107.
25. Benemei, S.; Fusi, C.; Trevisan, G.; Geppetti, P. The TRPA1 channel in migraine mechanism and treatment. Br J Pharmacol. 2014, 171(10), 2552–67.
26. Nummenmaa, E.; Hämäläinen, M.; Moilanen, L.J.; Paukkeri, E.L.; Nieminen, R.M.; Moilanen, T.; et al. Transient receptor potential ankyrin 1 (TRPA1) is functionally expressed in primary human osteoarthritic chondrocytes. Arthritis Res Ther. 2016, 18(1), 1–11.
27. Bessac BF, Sivula M, von Hehn CA, Caceres AI, Escalera J, Jordt SE. Transient receptor potential ankyrin 1 antagonists block the noxious effects of toxic industrial isocyanates and tear gases. FASEB J. 2009;23(4):1102-14.
28. Earley,S.; Brayden J.E. PhysiolTransient Receptor Potential Channels in the Vasculature. Physiol Rev. 2015, 95(2), 645-90.
29. Himmel, N.J; Cox, D.N. Transient receptor potential channels: current perspectives onTransient receptor potential channels: current perspectives on evolution, structure, function and nomenclature. Proc Biol Sci. 2020, 26, 287.
30. Salem, H. Ballantyne B. CS Gas. In: Wexler P, editor. Encyclopedia of Toxicology. 1. Oxford: Elsevier; 2005: 686-90
31. Quiroga-Garza, M.E.; Ruiz-Lozano R.E.; Azar, N.S.; Mousa, H.M.; Komai, S.; Sevilla-Llorca, J.L.; et al. Noxious effects of riot control agents on the ocular surface: Pathogenic mechanisms and management. Front Toxicol. 2023, 5.
32. Ilgaz, A.; Uyanusta, FÇK.; Arbak, P.; Müezzinoğlu, A.; Çiftçi, T.U.
; ; Akpınar, S.; et al. Extensive exposure to tear gases in ankara. Turkish Thorac J. 2019, 20(2), 108–13.
33. Schep, L.J.; Slaughter, R.J.; McBride, D.I. Riot control agents: The tear gases CN, CS and OC-a medical review. J R Army Med Corps. 2015, 161(2), 94–9.
34. Tsang, ACO.; Li, L.F.; Tsang, RKY. Health risks of exposure to CS gas (tear gas): An update for healthcare practitioners in Hong Kong. Hong Kong Med J. 2020, 26(2), 151–3.
35. Lam RPK, Wong KW, Wan CK. Allergic contact dermatitis and tracheobronchitis associated with repeated exposure to tear gas. Lancet. 2020, 396(10247), e12.
36. Torgrimson-Ojerio, B.N.; Mularski, K.S.; Peyton, M.R.; Keast, E.M.; Hassan, A.; Ivlev, I. Health issues and healthcare utilization among adults who reported exposure to tear gas during 2020 Portland (OR) protests: a cross-sectional survey. BMC Public Health. 2021, 21(1), 1–10.
37. Aykaç, N. Airway obstruction and patchy parenchymal infiltrations related to tear gas exposure. Duzce Med J. 2020, 22(2), 146–8.
38. Arbak, P.; Başer, I.; Kumbasar .ÖO.; Ülger, F.; Kiliçaslan, Z.; Evyapan, F. Long term effects of tear gases on respiratory system: Analysis of 93 cases. Sci World J. 2014, 2014, 5–9.
39. Brown, J.L.; Lyons, C.E.; Toddes, C.; Monko, T.; Tyshynsky, R. Tear gas safety and usage practices. J Sci Policy Gov. 2021, 18(01).
40. Carron, P.N.; Yersin, B. Management of the effects of exposure to tear gas. BMJ. 2009 Jun;338, b2283–b2283.
41. Tidwell, R.D.; Wills, B.K. Tear Gas and Pepper Spray Toxicity. StatPearls. 2023.
42. Engstrom, P. Disappearances in the post-transition era in Latin America. Int Aff. 2022 , 98(4), 1493–4.
43. The Minnesota Protocol on the Investigation of Potentially Unlawful Death 2016. Available on https://www.ohchr.org/sites/default/files/Documents/Publications/MinnesotaProtocol.pdf (accessed 10 julio 2023)
44. Hoz, S.S.; Aljuboori, Z.S.: Dolachee, A.A.; Al-Sharshahi, Z.F.; Alrawi, M.A.; Al-Smaysim, A.M. Fatal Penetrating Head Injuries Caused by Projectile Tear Gas Canisters. World Neurosurg. 2020, 138, e119–23.
45. Patai, S.; Rappoport, Z. 71. Nucleophilic attacks on carbon–carbon double bonds. Part II. Cleavage of arylmethylenemalononitriles by water in 95% ethanol. J Chem Soc. 1962, 383–91.
46. Frankenberg L, Sorbo B. Formation of cyanide from o-chlorobenzylidene malononitrile and its toxicological significance. Arch Toxikologie. 1973, 31(2), 99–108.
47. STERN, J. WEIL-MALHERBE, H.; GREEN, R.H. The effects and the fate of malononitrile and related compounds in animals tissues. Biochem J. 1952, 52(1) 114–25.
48. NATIONAL TOXICOLOGY PROGRAM Technical Report Series No. 377 TOXICOLOGY AND CARCINOGENESIS STUDIES OF CS2 IN F344/N RATS AND B6C3Fi MICE (INHALATION STUDIES). Available from: moz-extension://895e667a-16b1-4503-82c2-0061d12ddf18/enhanced- (accessed on 4 de septiembre 2023)
49. Von Stackleberg K, Amos C, Smith T, Cropek D, Macallister B. Military Smokes And Obscurants Fate And Effects A Literature Review Relative to Threatened and Endangered Species. 2004. Available from: https://www.researchgate.net/publication/235101035_Military_Smokes_and_Obscurants_Fate_and_Effects_A_Literature_Review_Relative_to_Threatened_and_Endangered_Species ( accessed 15 de julio 2023)
50. Committee on Acute Exposure Guideline Levels Committee on Toxicology Board on Environmental Studies and Toxicology Division on Earth and Life Studies. 2014. Available from: http://www.nap.edu/ (accessed 15 de julio 2023).
Received: 25 June 2023/ Accepted: 26 August 2023 / Published:15 September 2023
Citation: Caballero C, Sosa L, Puerto Sanabria C, Alvarenga Arriaga N, Alvarenga Arriaga V, Coca C, Rodriguez F. El 2-Clorobenzilideno Malononitrilo como agente antidisturbios: generalidades y sus efectos en el hombre Revis Bionatura 2023;8 (3) 82. http://dx.doi.org/10.21931/RB/2023.08.03.82.
