Revision/Review
Files > Volume 1 > Vol 1 No 2 2016 > Revisiones
Mecanismos de invasion del esporozoíto y merozoíto de Plasmodium
Mechanisms of invasion from sporozoite and merozoíto of Plasmodium
Available from: http://dx.doi.org/10.21931/RB/2016.01.02.9 Lilian M. Spencer1,2, Andreina Gómez3, Eva Collovini4
Resumen
La malaria o paludismo en el humano es causada por cuatro especies de Plasmodium pertenecientes al phylum Aplicomplexa; ovale, malariae, vivax y falciparum, siendo esta última la responsable de las complicaciones clínicas más graves e incluso la muerte del hospedador vertebrado. El parásito Plasmodium posee organelos secretores especializados llamados rhoptrias, micronemas y gránulos densos, los cuales facilitan la invasión a las células hospedadoras.
El estadio de esporozoíto del Plasmodium migra y penetra a través de diferentes células en el hospedador vertebrado hasta llegar al hepatocito y formar la vacuola parasitófora; la ruptura del hepatocito libera otro estadio del parásito llamado merozoíto, el cual invade a los eritrocitos y también forma una vacuola parasitófora. Los investigadores proponen varios mecanismos de invasión como el movimiento de deslizamiento del esporozoíto (Gliding motility en Inglés), mientras que la invasión del merozoíto se realiza en tres pasos: contacto inicial, re-orientación e invasión. En esta revisión nos enfocamos en las proteínas de superficie tanto del esporozoíto como del merozoíto para el entendimiento de los mecanismos moleculares de la invasión hasta la elaboración de la vacuola parasitófora. Se hace referencia a las proteínas mas importantes que intervienen en estos mecanismos y son posibles candidatas en el diseño de una vacuna anti-malárica.
Palabras clave: malaria, invasión, esporozoíto, merozoíto, Plasmodium.
Abstract
Malaria or paludismo is caused in humans by four species of Plasmodium belonging to phylum Apicomplexa: ovale, malaria, vivax and falciparum, being the last, the responsible of the clinical complication and death in the vertebrate host. Plasmodium parasite possess a specialized secretory organelles called rhoptries, micronemes and dense granules that facilitate invasion of host cells.
The sporozoite stage of Plasmodium travels through the different cells of vertebrate host until it reaches the hepatocyte and have been form the parasitophorous vacuole. The infected hepatocytes rupture, results in the releasing thousands of daughter merozoites that invade the erythrocytes with the formation of parasitophorous vacuole too.
Several researchers suggest the gliding motility mechanism as the responsible of hepatocyte invasion. While, which the erythrocyte invasion process has been described as the result of tree steps: first contact, re-orientation and invasion.
In this review the surface proteins of merozoites and esporozoites are pointed out as the most important factors for the molecular invasion mechanisms until the elaboration of the parasitophorous vacuole. These proteins that take part in these mechanisms are the possible candidates in the design of an anti-malaria vaccine.
Key words: malaria, invasion, esporozoíto, merozoíto, Plasmodium.
Introducción
La malaria o paludismo es causada por el parásito protozoario del género Plasmodium, perteneciente al phylum Aplicomplexa. Existen cinco especies que infectan al humano (hospedador vertebrado): ovale, malariae, vivax, falciparum y knowlesis. Esta última se reportó como una zoonosis de primates a humanos en regiones africanas1. La especie falciparum es la más agresiva en relación a las manifestaciones clínicas, y es responsable de la mayoría de las muertes en el hospedador humano. La Organización Mundial de la Salud en el 2011 reporto cerca de 216 millones de personas infectadas de malaria y aproximadamente 655.000 muertes. Se estima que la mitad de la población mundial está en riesgo de contraer la enfermedad, por lo que es una prioridad desarrollar estrategias para el diseño de una vacuna efectiva1. El parásito ha desarrollado una compleja estrategia para adaptarse a sus hospedadores y evadir el sistema inmune. Uno de los mecanismos recientemente descritos es la formación del merosoma, proceso por el cual, los merozoítos que salen del hígado, evaden el sistema inmune por estar dentro de una vesícula (merosoma) que se libera en los vasos sanguíneos del hígado (sinusoides) antes de invadir a los eritrocitos2.
Este parásito presenta un ciclo de vida muy complejo (Fig. 1). Los parásitos son transmitidos por un vector, la hembra del mosquito Anopheles, que es portador del parásito al alimentarse de la sangre de un vertebrado infectado. En el tubo digestivo del mosquito se lleva a cabo el ciclo sexual del parásito con la fecundación de los macro y micro gametos, y posteriormente se desarrolla el zigoto motil llamado ookineto. Una división asexual da origen al esporozoíto, que es el estadio infectante del vertebrado. Cuando los esporozoítos que están en las glándulas salivares del vector son inyectados dentro del hospedador vertebrado, son trasportados rápidamente al hígado donde invaden a los hepatocitos3, en los cuales ocurre una división asexual llamada esquizogonia hepática o ciclo extra-eritrocítico que da origen al estadio llamado merozoíto. Este proceso de invasión del esporozoíto ha sido extensivamente estudiado por varios investigadores4,5,6,7, aunque poco se sabe del desarrollo y liberación del merozoíto proveniente de las células hepáticas. En P. vivax se ha descrito otro estadio adicional llamado hipnozoíto, el cual queda latente en los hepatocitos y puede activar la infección en un periodo relativamente corto entre 10 a 30 semanas, siendo responsable de las recidivas de la enfermedad 8.
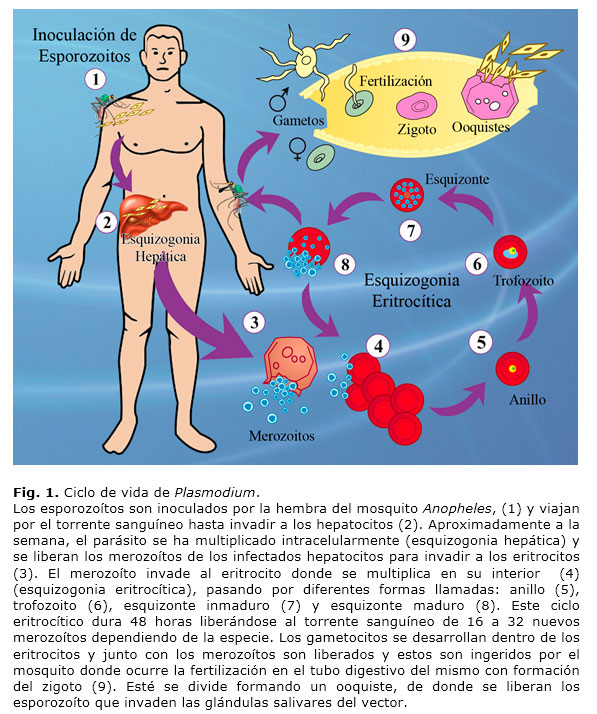
El merozoíto es liberado al torrente sanguíneo con consiguiente invasión de los eritrocitos en los cuales ocurre otra división asexual, llamada esquizogonia eritrocítica. El merozoíto comienza la invasión al eritrocito del cual se liberan más de 32 nuevos merozoítos en aproximadamente 48 horas, provenientes de un esquizonte maduro. Este esquizonte maduro estalla, liberando y dispersando los nuevos merozoítos que re-invaden nuevos eritrocitos. También, a partir del esquizonte maduro, se liberan al torrente sanguíneo los gametocitos, los cuales son ingeridos por el mosquito vector al picar al hospedador infectado y de esta forma se cierra el ciclo del parásito. En los procesos de invasión del esporozoíto y merozoíto están involucradas numerosas proteínas y solo en el merozoíto de P. falciparum se reportan más de 409. Estas proteínas no solo se encuentran distribuidas en la superficie de los diferentes estadios del parásito; sino también son secretadas por organelos especializados como micronemas, roptrias y gránulos densos que conforman parte del complejo apical y donde se presentan muchas de las proteínas necesarias para el proceso de invasión y el establecimiento de la vacuola parasitófora (VP) dentro de las células del hospedador10-12.
Se ha reportado un patrón de organización en las organelas que constituyen el complejo apical, el cual es muy similar tanto en el esporozoíto como en merozoíto (Fig. 2)13, 14.

En este trabajo se hará hincapié en las proteínas más relevantes implicadas en los mecanismos de invasión, tanto las del esporozoíto como del merozoíto de P. falciparum. En el primer caso las mas importantes son: la Proteína Anónima Relacionada con la Trombospondina (TRAP, del inglés thrombospondin-related anonymous protein), y la Proteína Circumesporozoitica (CSP, del inglés circumsporozoite protein); y en el merozoíto: el Antígeno de Membrana Apical 1 (AMA 1, del inglés apical membrane antigen 1), la Proteína de Superficie del Merozoíto 1 (MSP 1, del inglés merozoite surface protein 1) conocida también como el Antígeno de Superficie del Merozoíto 1 (MSA 1, del inglés merozoite surface antigen 1), y el Antígeno Unido al Eritrocito (EBA, del inglés erythrocyte binding antigen). Otras proteínas son representadas por la familia de Proteínas Roptrias (RAP, del inglés rhoptrias antigen protein), el Antígeno de Superficie del Eritrocito en Anillo Infectado (RESA, del inglés ring-infected erythrocyte surface antigen), el Antígeno de Membrana del Anillo (RIMA, del inglés ring membrane antigen) y dos proteasas parecidas a Subtilisina (SUB-1 y SUB-2, del inglés subtilisin-like porteases), siendo estas las más relevantes en la invasión y en el diseño de vacunas15.
Todas estas proteínas juegan un papel esencial para entender los mecanismos de invasión del parásito en las células del hospedador, y están involucradas tanto en el movimiento de desplazamiento del esporozoíto, como en la rápida penetración del merozoíto y en la interacción receptores-ligandos en la superficie del parásito hasta la formación de la VP.
Proteínas implicadas en el reconocimiento e invasión del hepatocito por el esporozoíto
El esporozoíto es el estadio con mejor adaptación ya que se puede encontrar en diferentes hospedadores y tipos de células. El esporozoíto de Plasmodium es móvil y presenta un movimiento característico en espiral descrito por varios investigadores llamado "Deslizamiento" (glinding motility en inglés). Este movimiento requiere de microfilamentos y es esencial para la invasión16.
En este proceso de invasión, la proteína CSP es esencial y se encuentra en mayor proporción en la superficie del parásito por medio de un anclaje tipo glicosil fosfatidil inositol (GPI, del inglés glycosil phosfatil inositol) a la membrana del esporozoíto. Esta CSP es expresada desde el estadio de ooquiste dentro del vector y presenta una secuencia repetida de amino ácidos (NANP), que fue usada en el primer ensayo de vacuna para malaria17,18. Varios investigadores han demostrado que la CSP está presente en el citosol de los hepatocitos cuando se incuban con esporozoítos 4. Esta proteína contiene una copia de la proteína trombospondina (TSP) tipo I de humano y es translocada a la superficie por un proceso dependiente de actina16.
El parásito en las glándulas salivares del vector inicia la expresión de las proteínas TRAP y CSP. La TRAP se localiza en los micronemas y es secretada sobre la superficie del parásito. Esta proteína contiene una estructura con una secuencia señal de amino ácidos hidrofóbica la cual ha sido encontrada en algunas integrinas (región II), es rica en prolina y presenta una cola hidrofílica citoplasmática19. Experimentos de inmunofluorescencia con anticuerpos han demostrado que en el momento de la invasión hay una relocalización de la proteína TRAP sobre el parásito concentrándose en un extremo en forma de capuchón20 Sin embargo, TRAP parece no ser determinante en la invasión y presenta una función primordial en el proceso de adhesión ya que reconoce a la molécula de heparin sulfato (HS) de los hepatocitos. La CSP como la TRAP, reconoce diferentes tipos específicos de proteoglicanos (HSPG, del inglés highly sulfated heparin sulfate proteoglycans) en la superficie celular de las células de Kupffer, células estrelladas y hepatocitos; pero no del endotelio sinusoidal21.
Noe y Adams22, demostraron por confocalidad que la proteína de Membrana Apical Antígeno/Unida al Eritrocito (MAEBL, del inglés apiacal membrane antigen/erythrocyte binding-like protein), localizada en las roptrias, se expresa junto con las proteínas roptrias 1 y 2 (RAP 1 y RAP 2, del inglés rhoptry associated protein 1 and 2) involucradas en el proceso de invasión. Esta proteína es expresada relativamente temprano en el desarrollo del esquizonte, apareciendo sobre la superficie del merozoíto; su función todavía no ha sido aclarada.
Cuando el esporozoíto entra al torrente sanguíneo es capaz de penetrar en el hepatocito induciendo la invaginación de la membrana plasmática (MP) y la formación de la VP para multiplicarse en el interior de la célula del hospedador.
La pregunta lógica que se hicieron los investigadores que estudian los mecanismos de invasión del esporozoíto después de dilucidar los procesos de adhesión entre las células parásito-hospedador, fue: ¿cómo migra el esporozoíto desde el vaso sinusoidal al hepatocito?
Se sabe que existe un marcado tropismo entre el esporozoíto y el hepatocito que esta cubierto por HSPGs del tipo HS, los cuales son abundantes en la matriz extracelular de los hepatocitos y estos a la vez tienen interacción con la CSP23, 24. La CSP también reconoce a las HSPGs de las células de Kupffer y estrelladas que están en el espacio de Disse. Uno de los modelos planteados es que el esporozoíto es arrastrado desde el vaso sanguíneo sinusoide hacia la matriz extracelular y a las células de Kupffer, residentes de los vasos sinusoides, por la unión establecida con los HSPGs y de esa forma atraviesa la barrera de la célula sinusoidal25, 26. Pradel y Frevert en el 2001 25, demostraron que el esporozoíto pasa primero por la célula de Kupffer y luego al hepatocito, lo que sugiere que la célula de Kupffer presenta actividad fagocítica actuando como un transportador del esporozoíto.
Pradel y colaboradores21, proponen otro modelo para explicar la invasión del hepatocito por el esporozoíto, sugiriendo que los esporozoítos se unen a los HPSGs que están proyectados hacia el espacio de Disse de la matriz extracelular y atraviesan el endotelio fenestrado siendo arrastrados desde el sinusoide al hepatocito. En la figura 3, se presenta un modelo de cómo los HSPGs de la superficie de las células de Kupffer intervienen en el proceso de migración de los esporozoítos por medio de un mecanismo de extravasión celular donde el parásito penetra al parénquima de la célula hepática. La teoría mas aceptada hoy en día es que la invasión esta mediada por las células de Kupffer que actúan como transportadora.

Proteínas del merozoíto implicadas en el reconocimiento e invasión al eritrocito
Tanto el esporozoíto como el merozoíto presentan un complejo apical que secreta su contenido durante la invasión a las células del hospedador (Fig. 2). Los mecanismos de invasión del merozoíto al eritrocito no están completamente dilucidados. Se ha establecido que la invasión del merozoíto es un proceso muy rápido de aproximadamente 20 segundos con una secuencia de eventos que se pueden resumir en 4 pasos: (1) contacto del merozoíto con el eritrocito por cualquier parte de la superficie del parásito; (2) orientación del extremo apical hacia la membrana del eritrocito; (3) ataque del complejo apical desplazándose dentro de la célula hospedadora y la unión entre las membranas de ambas células; (4) proceso de internalización del merozoíto por el motor actina/miosina y al mismo tiempo la formación de la VP12.
Este complejo apical juega un papel esencial en la invasión, ya que el contenido de las roptrias y micronemas es secretado promoviendo una fuerte unión entre la superficie del merozoíto y la membrana del eritrocito27. Esta unión genera una fuerza de penetración mediada por la interacción de las moléculas de actina/miosina del citoesqueleto del parásito y algunas proteínas de la superficie del eritrocito, resultando como producto final del proceso, la formación de la VP donde reside el parásito para multiplicarse asexualmente 28. La VP actúa como una barrera semipermeable entre el parásito y el eritrocito permitiendo la adquisición de nutrientes y secreción de proteínas derivadas del parásito. Por lo tanto, la esquizogonia eritrocítica es la parte del ciclo de vida del parásito donde se inicia el desarrollo de estructuras en el eritrocito anucleado hasta formarse el esquizonte maduro con la consecuente liberación de nuevos merozoítos 29(Fig. 1).
Muchas proteínas del merozoíto están involucradas en este proceso, pero muy poco se sabe de su papel en la invasión. En la siguiente tabla presentamos algunas de las proteínas más estudiadas para el diseño de vacunas aunque no están todas ya que cada día se reportan nuevas cantidades en busca de una respuesta inmunologíca efectiva (Tabla). Entre las proteínas involucradas la MSP-1 está relacionada en la interacción inicial con el eritrocito30,31. Esta proteína está unida a la superficie del merozoíto por un anclaje tipo GPI, al igual que las MSP-2, MSP-4 y MSP-532-34. La MSPs son un complejo de proteínas que sufren varios procesos proteolíticos como la MSP-1 dando una serie de polipéptidos, y siendo el péptido de 19 kDa el que permanece unido a la MP del parásito por su extremo carboxílico. Recientemente se han descrito dos proteasas la SUB-1 y 2 que han sido localizadas en los gránulos densos y han sido postuladas como las responsables del clivaje de la MSP-1 en la invasión35.

La proteína denominada AMA1, una proteína integral de membrana, se localiza inicialmente en el cuello de las roptrias y, después de la ruptura del esquizonte, se localiza en la superficie del parásito y su función no ha sido determinada29, 36.
Otra proteína secretada por los gránulos densos es la RIMA de 14 kDa en P. falciparum. Esta proteína cuya función no ha sido completamente dilucidada, es expresada en el equizonte tardío y en los merozoítos libres y está localizada sobre la membrana de las nuevas formas de anillo justo después de la invasión, la función no ha sido dilucidada37.
En las roptrias, además de la AMA 1 se han identificado varias proteínas, (Proteínas Asociadas a Roptrias 1 y 2, RAP 1 y RAP 2; y otra menos estudiada RAP-3) formando un complejo, las cuales pueden estar involucradas en la invasión y han sido observadas en la VP en el proceso de penetración al eritrocito10, 38,39,40. Las RAP 1 y 2 fueron aisladas por primera vez en merozoítos de P. knowlesi como una molécula de 66 kDa y fueron las primeras proteínas secuenciada en roptria y localizadas en el conducto de la organela41.
La proteína antigénica unida al Eritrocito (EBA-175, del inglés erythrocyte binding antigen 175), se ubica en los micronemas y se une a la molécula de Glicoforina A por medio de ácidos siálicos, los cuales generan una carga negativa y por lo tanto está relacionada en el contacto inicial entre el parásito y el eritrocito42-44. Otra proteína llamada EBA-140 (también conocida como BAEBL) ha sido identificada en la invasión, uniéndose a la molécula de Glicoforina C del eritrocito45,46. Estos hallazgos indican que las moléculas de Glicoforinas A, B y C de la superficie del eritrocito están presentes en relativa abundancia y son los receptores que median el contacto inicial con el parásito.
En el parásito sólo cuatro proteínas localizadas en los gránulos densos del complejo apical han sido identificadas, siendo el antígeno de superficie del eritrocito en forma de anillo infectado (RESA, del inglés ring-infected erythrocyte surface antigen,) el más relevante como candidato a vacuna. Esta proteína es secretada al mismo tiempo que ocurre la invasión, translocándose a través de la membrana de la VP y localizándose bajo la membrana del eritrocito parasitado en asociación con el citoesqueleto37,47. Esta se expresa en el esquizonte tardío y es almacenada en la organela hasta la invasión cuando es liberada.
P. vivax , la otra especie del parásito que es responsable de las manifestaciones clínicas graves en el humano, además de presentar las proteínas antes mencionadas que están conservadas en todas las especies, invade a los reticulocitos (eritrocitos inmaduros), los cuales presentan un grupo de moléculas llamadas receptores Duffy o antígenos Duffy unidas a otras proteínas denominadas proteínas similares a las unidas a Duffy (DBP, del inglés Duffy bindind protein) presentes en las roptrias del merozoíto45. La población negra no presenta infecciones por P. vivax porque sus eritrocitos carecen de estos receptores. La familia de proteínas DBL y las proteínas de 235 kDa localizadas en micronemas y roptrias respectivamente intervienen en la selección del tipo de eitrocito a invadir por el merozoíto. Sin embargo otros estudios en modelos experimentales con ratones han mostrado que la MSP-749 y la MSP-850 están involucradas en la selección de los eritrocitos a invadir.
Las proteínas involucradas en los mecanismos de invasión del parásito en sus diferentes estadios infectantes y sus modificaciones, son estrategias empleadas para cito-adherirse a diferentes tipos de células hospedadoras y multiplicarse en ellas. Los conocimientos de estas proteínas pueden ser utilizados en el desarrollo de fármacos y en el diseño de vacunas antimaláricas.
Conclusiones
El estadio inicial de malaria incluye la migración de los esporozoítos de la piel al hígado, la invasión de los hepatocitos y subsecuentemente el desarrollo del parásito al estadio de merozoíto. Estos pasos obligatorios para establecer una infección exitosa en el hospedador vertebrado involucran una serie de proteínas que son esenciales en los mecanismos de invasión del Plasmodium a las células del hospedador como son las proteínas parecidas a Subtilisina (SUB-1 y SUB-2), RESA, CSP, TRAP y las MSPs. La aplicación lógica de estos conocimientos es una herramienta básica para la selección de una o unas proteínas candidatas a vacuna y control terapéutico para la enfermedad, por lo que se requiere un profundo entendimiento de los complejos moleculares y los procesos que están relacionados en la invasión celular en malaria.
Agradecimientos
Le agradecemos al Decanato de Investigación y Desarrollo de la Universidad Simón Bolívar (DID-USB) por apoyar la búsqueda de información para la realización de este artículo. Nosotros nos disculpamos con los investigadores que trabajan en esta área y no han sido citados en este trabajo por límite de espacio. También queremos agradecerle a Alberto Louro por su crítica revisión del manuscrito.
Referencias bibliográficas
- World Health Organization: World Malaria Report 2011. http://www.who.int/malaria/world_malaria_report_2011/
- Sturm A, Amino R, van de Sand C, Regen T, Retzlaff S, Rennenberg A, Krueger A, Pollok JM, Menard R, Heussler VT. (2006) Manipulation of host hepatocytes by the malaria parasite for delivery into liver sinusoids. Science. 313(5791):1287-90.
- Sinden RE (2002) Molecular interactions between Plasmodium and its insect vectors. Cell Microbiol. 4: 713-724.
- Mota MM, Pradel G, Vanderberg JP, Hafalla JC, Frevert U, Nussenzweig RS, Nussenzweig V, Rodriguez A (2001) Migration of Plasmodium sporozoites through cells before infection. Science 291: 141-144.
- Matuschewski K, Nunes AC, Nussenzweig V, Menard R (2002) Plasmodium sporozoite invasion into insect and mammalian cells is directed by the same dual binding system. EMBO J. 21: 1597-1606.
- Baldacci P, Menard R (2004) The elusive malaria sporozoite in the mammalian host. Mol. Microbiol. 54: 298-306.
- Prudêncio M and Mota M (2007). To Migrate or to Invade: Those Are the Options. Cell Host Microbe 2: 286-288.
- Garnham PCC (1988). Hypnozoites and "relapses" in Plasmodium vivax and in vivax-like malaria. Trop. Geogr. Med. 40: 187-195.
- Cowman AF, Crabb BS (2006) Invasion of red blood cells by malaria parasites. Cell 124: 755-766.
- Bannister LH, Hopkins JM, Fowler RE, Krishna S, Mitchell GH (2000a) Ultrastructure of rhoptry development in Plasmodium falciparum erythrocytic schizonts. Parasitology 121: 273-287.
- Kats LM, Black CG, Proellocks NI, Coppel RL (2006) Plasmodium rhoptries: how things went pear-shaped. Trends Parasitol. 22: 269-276.
- Kats LM, Cooke BM, Coppel RL, Black CG (2008) Protein trafficking to apical organelles of malaria parasites - Building an invasion machine. Traffic 9: 176-186.
- Bannister LH, Hopkins JM, Fowler RE, Krishna S, Mitchell GH (2000b) A brief illustrated guide to the ultrastructure of Plasmodium falciparum asexual blood stages. Parasitol. Today 16: 427-433.
- Schrevel J, Asfaux-Foucher G, Hopkins JM, Robert V, Bourgouin C, Prensier G, Bannister LH (2007) Vesicle trafficking during sporozoite development in Plasmodium berghei: ultrastructural evidence for a novel trafficking mechanism. Parasitology 135 : 1-12.
- Preiser P, Kaviratne M, Shahid Khan S, Lawrence Bannister L, Jarra W (2000) The apical organelles of malaria merozoites: host cell selection, invasion, host immunity and immune evasion. Microbes Infect. 2: 1461-1477.
- Stewart MJ, Vanderberg JP (1991). Malaria sporozoites release circumsporozoite protein from their apical end and translocate it along their surface. J. Protozool. 38: 411-421.
- Ballou WR, Hoffman SL, Sherwood JA, Hollingdale MR, Neva FA, Hockmeyer WT, et al. (1987) Safety and efficacy of a recombinant DNA Plasmodium falciparum sporozoite vaccine. Lancet 1: 1277-81.
- Posthuma G, Meis JF, Verhave JP, Hollingdale MR, Ponnudurai T, Meuwissen JH, Geuze HJ (1988) Immunogold localization of circumsporozoite protein of the malaria parasite Plasmodium falciparum during sporogony in Anopheles stephensi midguts. Eur. J. Cell Biol. 46:18-24.
- Dolo A, Modiano D, Doumbo O, Bosman A, Sidibé T, Keita MM, Naitza S, Robson KJ, Crisanti A (1999) Thrombospondin related adhesive protein (TRAP), a potential malaria vaccine candidate. Parassitologia 41:425-8.
- Mota MM, Rodriguez A (2001) Migration through host cells by apicomplexan parasites. Microbes infect. 3: 1123-1128.
- Pradel G, Garapaty S, Frevert U (2002) Proteoglycans mediate malaria sporozoite targeting to the liver. Mol. Microbiol. 45: 637-651.
- Noe AR, Adams JH (1998) Plasmodium yoelii YM MAEBL protein is coexpressed and colocalizes with rhoptry proteins. Mol. Biochem. Parasitol. 96: 27-35.
- Pinzon-Ortiz C, Friedman J, Esko J, Sinnis P (2001). The binding of the circumsporozoites protein to cell surface heparan sulfate proteoglycans is required for Plasmodium. J. Biol. Chem. 276: 26784- 26791.
- Sinnis P, Coppi A (2007) A long and winding road: the Plasmodium sporozoite's journey in the mammalian host. Parasitol. International 56: 171-178.
- Pradel G, Frevert U (2001) Malaria sporozoites actively enter and passage through Kupffer cells prior to hepatocyte invasion. Hepatology 33: 1154-1165.
- Shin S, Vanderberg J, Terzakis J (1982). Direct Infection of hepatocytes by sporozoites of Plasmodium berghei. The Journal Protozoology 11 : 352-359.
- Gratzer WB, Dluzewski AR (1993) The red blood cell and malaria parasite invasion. Semin. Hematol. 30: 232-247.
- Cowman AF, Baldi DL, Healer J, Mills KE, O'Donnell RA, Reed MB, Triglia T, Wickham ME, Crabb BS (2000) Functional analysis of proteins involved in Plasmodium falciparum merozoite invasion of red blood cells. FEBS Lett. 476: 84-88.
- Bannister LH, Dluzewski AR (1990) The ultrastructure of red cell invasion in malaria infections: a review. Blood Cells 16: 257-292.
- Holder AA, Freeman RR (1984) The three major antigens on the surface of Plasmodium falciparum merozoites are derived from a single high molecular weight precursor. J. Exp. Med. 160: 624- 629.
- Holder AA, Blackman MJ (1994) What is the function of MSP-1 on the malaria merozoite?. Parasitol. Today. 10:182-184.
- Smythe JA, Coppel RL, Brown GV, Ramasamy R, Kemp DJ, Anders RF (1988) Identification of two integral membrane proteins of Plasmodium falciparum. Proc. Natl. Acad. Sci. USA 85: 5195-5199.
- Marshall VM, Silva A, Foley M, Cranmer S, Wang L, McColl DJ, Kemp DJ, Coppel RL (1997) A second merozoite surface protein (MSP-4) of Plasmodium falciparum that contains an epidermal growth factor-like domain. Infect. Immun. 65: 4460-4467.
- Marshall VM, Tieqiao W, Coppel RL (1998) Close linkage of three merozoite surface protein genes on chromosome 2 of Plasmodium falciparum. Mol. Biochem. Parasitol. 94: 13-25.
- Barale J.C., Blisnick T., Fujioka H., Alzari P.M., Aikawa M., Braun-Breton C., Langsley G.(1999) Plasmodium falciparum subtilisin-like protease 2, a merozoite candidate for the merozoite surface protein 1-42 maturase. Proc. Natl. Acad. Sci. USA 96: 6445-6450.
- Miller LH, Aikawa M, Johnson JG, Shiroishi T (1979) Interaction between cytochalasin B-treated malarial parasites and erythrocytes. Attachment and junction formation. J. Exp. Med. 149: 172-184.
- Trager W, Rozario C, Shio H, Williams J, Perkins ME. (1992) Transfer of a dense granule protein of Plasmodium falciparum to the membrane of ring stages and isolation of dense granules. Infect. Immun. 60: 4656-4661.
- Aikawa M, Miller LH, Johnson J, Rabbege J (1978) Erythrocyte entry by malarial parasites. A moving junction between erythrocyte and parasite. J. Cell Biol. 77: 72-82.
- Bannister LH, Butcher GA, Dennis ED, Mitchell GH (1975) Structure and invasive behaviour of Plasmodium knowlesi merozoites in vitro. Parasitology 71: 483-491.
- Iyer J, Grüner AC, Renia L, Snounou G, Preiser PR (2007) Invasion of host cells by malaria parasites: a tale of two protein families. Mol. Microbiology 65: 231-249.
- Crewther PE, Culvenor JG, Silva A, Cooper JA, Anders RF (1990) Plasmodium falciparum: two antigens of similar size are located in different compartments of the rhoptry. Exp. Parasitol. 70:193-206.
- Camus D, Hadley TJ (1985) A Plasmodium falciparum antigen that binds to host erythrocytes and merozoites. Science 230: 553-556.
- Mayer DCG, Kaneko O, Hudson-Taylor DE, Reid ME, Miller LH (2001) Characterization of a Plasmodium falciparum erythrocyte-binding protein paralogous to EBA-175. Proc. Natl. Acad. Sci. U. S. A. 98: 5222-5227.
- Sim BKL, Carter JM, Deal CD, Holland C, Haynes JD, Gross M (1994) Plasmodium falciparum: further characterization of a functionally active region of the merozoite invasion ligand EBA-175. Exp. Parasitol. 78: 259-268.
- Narum DL, Fuhrmann SR, Luu T, Sim BKL (2002) A novel Plasmodium falciparum erythrocyte binding protein-2 (EBP2/BAEBL) involved in erythrocyte receptor binding. Mol. Biochem. Parasitol. 119: 159-168.
- Thompson JK, Triglia T, Reed MB, Cowman AF (2001) A novel ligand from Plasmodium falciparum that binds to a sialic acid-containing receptor on the surface of human erythrocytes. Mol. Microbiol. 41: 47-58.
- Rug M, Wickham ME, Foley M, Cowman AF, Tilley L. (2004) Correct promoter control is needed for trafficking of the ring-infected erythrocyte surface antigen to the host cytosol in transfected malaria parasites. Infect Immun. 72(10):6095-105.48.
- Galinski MR, Barnwell JW (1996) Plasmodium vivax: merozoites, invasion of reticulocytes and considerations for malaria vaccine development. Parasitol. Today 12: 20-29.
- Tewari, R., Ogun, S.A., Gunaratne, R.S., Crisanti, A., and Holder, A.A. (2005) Disruption of Plasmodium berghei merozoite surface protein 7 gene modulates parasite growth in vivo. Blood 105: 394-396.
- Shi, Q., Cernetich, A., Daly, T.M., Galvan, G., Vaidya, A.B., Bergman, L.W., and Burns, J.M., Jr (2005) Alteration in host cell tropism limits the efficacy of immunization with a surface protein of malaria merozoites. Infect. Immun. 73:6363-6371.
Recibido: 15 de marzo de 2016.
Aprobado: 30 de abril de 2016.
Aprobado: 30 de abril de 2016.
1 Departamento de Ciencias de la Vida y Biotecnología. Universidad Yachay Tech, Imbabura, Ecuador.
2 Universidad de Venezuela. Departamento de Biología Celular de la Universidad Simón Bólivar, Caracas-Venezuela.
3 Universidad de Granada, España.
4 Universidad Nacional Experimental Rómulo Gallego, Escuela Veterinaria, núcleo Zaraza, Venezuela.
Correspondencia: Lilian M. Spencer. Profesora del Departamento de Ciencias de la Vida y Biotecnología en Yachay Tech. E-mail: [email protected]; [email protected]
